..Redacción.
Johnson & Johnson ha anunciado que la Comisión Europea (CE) ha concedido la autorización de comercialización para la vacuna de Janssen Pharmaceutical Companies contra el ébola. Gracias a esta aprobación, Janssen está colaborando actualmente con la Organización Mundial de la Salud (OMS) con el objetivo de prevenir el ébola en países africanos, además de facilitar un acceso más amplio para aquellos que más lo necesitan.
Se presentaron dos solicitudes de autorización de comercialización (MAAs) a la Agencia Europea de Medicamentos (EMA) para las vacunas que componen la pauta de dos dosis, Zabdeno (Ad26.ZEBOV) y Mvabea (MVA-BN-Filo). Así, se ha concedido la autorización de comercialización bajo circunstancias excepcionales. Sin dejar de atender a la evaluación acelerada de las MAAs y de la opinión del Comité de Medicamentos de Uso Humano de la EMA. La pauta de vacunación frente al virus del ébola de Janssen está indicada para la inmunización. Asimismo combatir la especie Zaire ebolavirus en niños mayores de un año de edad y en adultos.
La vacuna tiene su origen en un programa de investigación en colaboración con los NIH
“La aprobación europea de la pauta de vacunación frente al virus del ébola de Janssen es un acontecimiento histórico. Lo es tanto para nuestra compañía como para la lucha mundial frente al virus mortal del Ébola. Partiendo de nuestra historia, estamos comprometidos con el desarrollo de vacunas que ayuden a superar la amenaza de algunas de las enfermedades infecciosas más letales del mundo”, ha declarado el doctor, principal responsable científico de Johnson & Johnson.
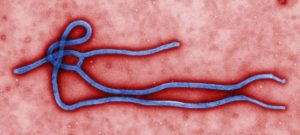 El peor brote de Ébola hasta la fecha fue la epidemia de África Occidental. Provocó cerca de 30.000 casos y más de 11.000 muertes entre 2014 y 2016. El segundo peor brote de Ébola registrado en el mundo comenzó en la República Democrática del Congo en 2018. Desde entonces ha causado más de 3.000 casos y más de 2.000 muertes, con una tasa de mortalidad del 65 %.
El peor brote de Ébola hasta la fecha fue la epidemia de África Occidental. Provocó cerca de 30.000 casos y más de 11.000 muertes entre 2014 y 2016. El segundo peor brote de Ébola registrado en el mundo comenzó en la República Democrática del Congo en 2018. Desde entonces ha causado más de 3.000 casos y más de 2.000 muertes, con una tasa de mortalidad del 65 %.“La aprobación de nuestra vacuna frente al ébola simboliza el avance en las vacunas potencialmente transformadoras. Sobre todo, a las comunidades con mayor riesgo de enfermedades infecciosas letales. No solo es la primera vacuna que surge de nuestra línea de desarrollo de vacunas. Se trata de la primera vacuna aprobada que se desarrolla gracias a la tecnología AdVac de Janssen. La misma tecnología se está utilizando para desarrollar candidatos a vacunas protectoras frente al SARS-CoV-2. Sin olvidarse de la vacuna para el Zika, VRS y VIH”, ha señalado el doctor Mathai Mammen, director global de Investigación y Desarrollo de Janssen, LLC.
La pauta de vacunación frente al Ébola de Janssen está diseñada específicamente para inducir inmunidad a largo plazo
La pauta de vacunación frente al ébola de Janssen está diseñada específicamente para inducir inmunidad a largo plazo. Se aplica en adultos y en niños mayores de un año de edad. Por lo tanto, se utilizará para apoyar la vacunación preventiva en países con mayor riesgo de brotes. Asimismo, en otros grupos de riesgo como trabajadores sanitarios, trabajadores de laboratorios, personal militar, personal de aeropuertos y visitantes a países de alto riesgo.
La pauta incluye Ad26.ZEBOV como primera dosis. Está basada en la tecnología del vector viral AdVac de Janssen. Por otro lado, MVA-BN-Filo como segunda dosis. Está basada en la tecnología MVA-BN® de Bavarian Nordic. Administrada en ocho semanas, aproximadamente.
“Estoy inmensamente agradecido a la dedicación de todos los que han formado parte de este desarrollo. A nuestros numerosos socios estratégicos globales, por su compromiso extraordinario para ayudar a hacer que esta pauta de vacunación fuera una realidad”, ha declarado el doctor Johan Van Hoof, director gerente de Janssen Pharmaceutical N.V.
Otro de los objetivos ha sido la vacunación en la RDC y en la vecina Ruanda
“El brote devastador de Ébola de 2014 en África Occidental creció exponencialmente, sobrepasando a los sistemas sanitarios. En menos de seis años, con el impulso de las colaboraciones público-privadas globales, tenemos una vacuna aprobada frente al Ébola que podría ayudar a aquellos que más la necesitan. Todo esto con el objetivo último de prevenir los brotes antes de que comiencen”, sentencia el director.
Otro de los objetivos ha sido la vacunación en la RDC y en la vecina Ruanda. Las compañías buscan prevenir la expansión geográfica del Ébola más allá de la zona del brote. Si se tienen en cuenta tanto los estudios clínicos como las iniciativas de vacunación, aproximadamente 60.000 personas han sido vacunadas con la pauta de Janssen frente al Ébola hasta la fecha.
En la misma línea, se han publicado ensayos clínicos de fase 1 promovidos por Janssen en revistas. Además han contado con revisión por pares como JAMA3 y el Journal of Infectious Diseases. Se presentaron datos de fase 1, 2 y 3 en el Congreso Europeo de Microbiología Clínica y Enfermedades Infecciosas. Estos estudios indican que la pauta de vacunación se tolera bien. Se han registrado respuestas inmunitarias robustas y duraderas a la especie Zaire ebolavirus. La evaluación del efecto protector de la pauta de vacunación se demostró a través de la vinculación de los resultados de inmunogenicidad clínica. La eficacia y los datos de inmunogenicidad obtenidos en primates no humanos.
La Iniciativa de Medicamentos Innovadores (IMI) proporcionó financiación a través del programa IMI Ebola para el lanzamiento de la vacuna
En mayo de 2019, el Grupo Asesor Estratégico de Expertos (SAGE) sobre inmunización de la OMS recomendó el uso de la pauta de vacunación de Janssen frente al virus del Ébola. La compañía agradece a sus socios estratégico. Entre ellos, Bavarian Nordic A/S, la Autoridad de Investigación y Desarrollo Biomédicos Avanzados. Además de la Oficina de la Secretaría Adjunta para Preparación y respuesta del Departamento de Salud y Servicios Humanos de EE.UU., la Iniciativa de Medicamentos Innovadores (IMI) y los Institutos Nacionales de Salud del Departamento de Salud y Servicios Sociales de EE.UU.
Presentación de expedientes y estado de los registros
La decisión de autorización de la comercialización por parte de la Comisión Europea llega tras la concesión por parte del CHMP de una evaluación acelerada para las MAAs de la pauta de vacunación preventiva . Las MAAs están respaldadas por datos de once estudios clínicos de fase 1, 2 y 3. Se encargan de evaluar la seguridad y la inmunogenicidad de la pauta en más de 6.500 adultos y niños mayores de un año en estudios preclínicos de EE.UU., Europa y África. También, buscan el análisis de inmunobridging que comparan los resultados de los estudios de eficacia clínicos y preclínicos. Por otro lado, se han mantenido conversaciones con la Administración de Alimentos y Medicamentos de EE. UU. para definir los datos necesarios para la solicitud de licencia en EE.UU.
Noticias relacionadas:
- Johnson & Johnson dona más de 137.000 unidades de productos de higiene personal para la Comunidad de Madrid
- Actualmente hay 20 vacunas y numerosos medicamentos en desarrollo para la Covid-19
- 30 medicamentos y cuatro vacunas en desarrollo para hacer frente a la epidemia del Covid-19
- El CSIC investiga una vacuna para el coronavirus a partir del virus que erradicó la viruela












