..Redacción.
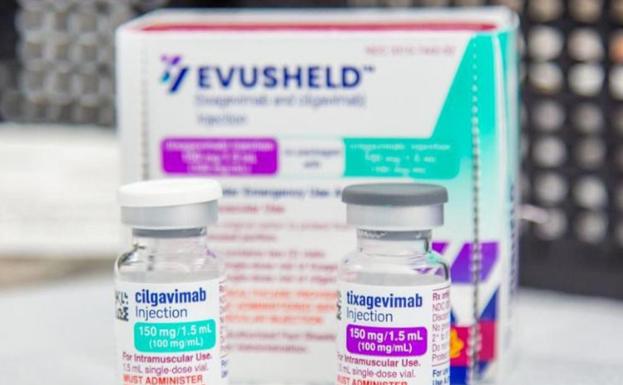
La Agencia Europea del Medicamento (EMA) ha recomendado la autorización de comercialización de Evusheld, como tratmeinto preventivo del Covid-19 en adultos y adolescentes a partir de 12 años y con al menos 40 kilos de peso. El tratamiento combinado de tixagevimab y cilgavimab y desarrollado por AstraZeneca se adhiere a la proteína spike para evitar que el virus del SARS-CoV-2 penetre en las células para multiplicarse. de manera que se evita la infección de Covid-19.
El Comité de Medicamentos Humanos (CHMP) de la EMA ha evaluado los datos de un estudio en más de 5.000 personas. Estos muestran que Evusheld, administrado en dos inyecciones de 150 mg de tixagevimab y 150 mg de cilgavimab, redujo el riesgo de infección por Covid-19 en un 77%. Asimismo, la duración de la protección del virus se estima en al menos seis meses.
De las personas que recibieron Evusheld, el 0,2% tuvieron un avance de Covid-19 confirmado por laboratorio después del tratamiento
En el estudio, los adultos que nunca habían tenido Covid-19 y que no habían recibido una vacuna contra el Covid-19 u otro tratamiento preventivo recibieron Evusheld o un placebo. De las personas que recibieron el fármaco, el 0,2% tuvieron un avance de Covid-19 confirmado por laboratorio después del tratamiento; en comparación con el 1% de las personas que recibieron placebo.
Por otro lado, el perfil de seguridad del fármaco de AstraZeneca fue favorable y los efectos secundarios fueron generalmente leves. Tan solo un pequeño número de personas informaron reacciones en el lugar de la inyección o hipersensibilidad.
El CHMP de la EMA enviará su recomendación a la Comisión Europea para una decisión rápida aplicable en todos los Estados miembros de la UE
Así, el CHMP concluye que los beneficios del medicamento son mayores que sus riesgos en el uso aprobado. Ahora enviará su recomendación a la Comisión Europea para una decisión rápida aplicable en todos los Estados miembros de la UE.
Por último, la EMA indica que los datos del estudio se han recopilado antes de la aparición de la variante Ómicron. Los estudios de laboratorio muestran que la variante Ómicron BA.1 puede ser menos sensible a tixagevimab y cilgavimab en dosis de 150 mg que la variante Ómicron BA.2. De modo que la EMA evaluará los datos en las próximas semanas. La idea es analizar si un régimen de dosificación alternativo podría ser apropiado para la prevención de Covid-19 ante variantes emergentes.
Noticias complementarias
- Sanidad aprueba Evusheld para mayores de 18 años con inmunodepresión grave que no respondan a la vacuna
- La combinación de anticuerpos de acción prolongada Evusheld de AstraZeneca mantiene la actividad neutralizante contra la variante Ómicron
- Sanidad acuerda con AstraZeneca el suministro de su anticuerpo monoclonal para prevenir el Covid-19 en pacientes inmunocomprometidos