..Redacción.
El tratamiento con pembrolizumab, un anti-PD-1 de la biofarmacéutica MSD, ha sido aprobado por la Comisión Europea como tratamiento adyuvante para adultos con melanoma en estadio III, afectación de los ganglios linfáticos y que se han sometido a resección quirúrgica completa. La aprobación permite la comercialización del fármaco para esta nueva indicación en los 28 estados miembros de la UE más Islandia, Liechtenstein y Noruega en la dosis aprobada de 200 mg cada tres semanas. Pembrolizumab, comercializado como Keytruda, también está aprobado en Europa como monoterapia para el tratamiento del melanoma avanzado (no resecable o metastásico) en adultos.
Los datos mostraron que pembrolizumab redujo el riesgo de recurrencia o muerte en un 44% en comparación con placebo
 Los datos aportados en el ensayo pivotal fase 3 EORTC1325/KEYNOTE-054, realizado a petición de la Agencia Europea del Medicamento (EMA) y en colaboración con la Organización Europea para la Investigación y el Tratamiento del Cáncer (EORTC, por sus siglas en inglés), mostraron que pembrolizumab prolongó de forma significativa la supervivencia libre de recurrencia (SLR), reduciendo el riesgo de recurrencia de la enfermedad o muerte en un 44% en comparación con placebo en la población general de pacientes con melanoma en estadio III resecado de alto riesgo.
Los datos aportados en el ensayo pivotal fase 3 EORTC1325/KEYNOTE-054, realizado a petición de la Agencia Europea del Medicamento (EMA) y en colaboración con la Organización Europea para la Investigación y el Tratamiento del Cáncer (EORTC, por sus siglas en inglés), mostraron que pembrolizumab prolongó de forma significativa la supervivencia libre de recurrencia (SLR), reduciendo el riesgo de recurrencia de la enfermedad o muerte en un 44% en comparación con placebo en la población general de pacientes con melanoma en estadio III resecado de alto riesgo.
El doctor Scot Ebbinghaus, vicepresidente de investigación clínica de MSD Research Laboratories, comentó que “el compromiso a largo plazo de MSD con los pacientes que padecen melanoma incluye un enfoque particular en la incorporación de nuevas opciones de tratamiento más tempranas a estos pacientes en el paradigma del tratamiento”. Además, esta aprobación “se asienta sobre las bases establecidas por pembrolizumab en el contexto del melanoma avanzado y metastásico”, añadió el Dr. Ebbinghaus.
 Dr. Ebbinghaus (MSD): “Esta aprobación se asienta sobre las bases establecidas por pembrolizumab en el contexto del melanoma avanzado y metastásico”
Dr. Ebbinghaus (MSD): “Esta aprobación se asienta sobre las bases establecidas por pembrolizumab en el contexto del melanoma avanzado y metastásico”
Por su parte, el doctor Alexander Eggermont, líder del estudio y director general del Instituto Oncológico Gustave Roussy, explicó que los pacientes que presentan melanoma y especialmente los que tienen la enfermedad en estadio III, “a menudo tienen un alto riesgo de recurrencia”, por lo que el estudio que están desarrollando de manera conjunta la EORTC y MSD “mostró una reducción en el riesgo de recidiva del cáncer tras la cirugía”.
Combatir las células tumorales
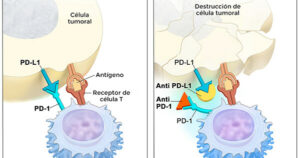
El principio activo pembrolizumab actúa aumentando la capacidad del sistema inmunitario del cuerpo para ayudar a detectar y combatir a las células tumorales. Se trata de un anticuerpo monoclonal humanizado que bloquea la interacción entre PD-1 y sus ligandos, PD-L1 y PD-L2, de tal forma que activa los linfocitos T y esto puede afectar tanto a las células tumorales como a las células sanas.
En España también se utiliza en monoterapia para la indicación en cáncer de pulmón no microcítico (CPNM) localmente avanzado o metastásico en adultos
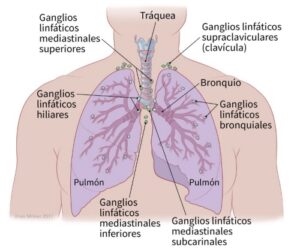 En España, este fármaco está financiado por el Sistema Nacional de Salud (SNS) en las siguientes indicaciones: en monoterapia, para el tratamiento de melanoma avanzado en adultos y para el tratamiento de primera línea del cáncer de pulmón no microcítico (CPNM) metástasico en adultos cuyos tumores expresen Pd-L1 con una proporción de marcador tumoral (TPS, por sus siglas en inglés) ≥50% sin mutaciones tumorales positivas de EGFR o ALK.
En España, este fármaco está financiado por el Sistema Nacional de Salud (SNS) en las siguientes indicaciones: en monoterapia, para el tratamiento de melanoma avanzado en adultos y para el tratamiento de primera línea del cáncer de pulmón no microcítico (CPNM) metástasico en adultos cuyos tumores expresen Pd-L1 con una proporción de marcador tumoral (TPS, por sus siglas en inglés) ≥50% sin mutaciones tumorales positivas de EGFR o ALK.
También se utiliza en monoterapia para la indicación en cáncer de pulmón no microcítico (CPNM) localmente avanzado o metastásico en adultos cuyos tumores expresen PD-L1 con una TPS ≥1% y que hayan recibido al menos un tratamiento de quimioterapia previo. Los pacientes con mutaciones de EGFR o de ALK también deben haber recibido terapia dirigida para estas alteraciones antes de recibir pembrolizumab.










