..Gema Maldonado.
César de la Fuente es profesor catedrático en la Escuela de Ingeniería y Ciencias Aplicadas de la Universidad de Pensilvania, donde ha diseñado y aplicado algoritmos de inteligencia artificial que han permitido identificar 2.603 péptidos potenciales antibióticos encriptados en proteínas del cuerpo humano que tienen funciones biológicas que nada tienen que ver con el sistema inmune. Junto a su equipo del grupo de Biología Computacional y otros colaboradores, ha demostrados que estos péptidos antibióticos “escondidos” son capaces de matar bacterias patógenas, dificultan posibles resistencias bacterianas y muestran actividad frente a infecciones en modelos de ratones. Además, probaron in vitro que la mezcla de péptidos antibióticos mejora la actividad antimicrobiana.
César de la Fuente ha descubierto miles de péptidos antibióticos en proteínas más grandes del cuerpo humano aplicando algoritmos de inteligencia artificial
Estos hallazgos han sido publicados en la revista Nature Biomedical Engineering. El trabajo dirigido por De la Fuente aplica un nuevo enfoque utilizando la bioinformática con el que los investigadores creen que se abren nuevas vías para hallar nuevos antibióticos. El Covid-19 ha sacado del foco una de las grandes amenazas para la humanidad: las resistencias antimicrobianas. Según estimaciones de Naciones Unidas, pueden ser la causante de 10 millones de muertes en 2050, más que el cáncer, si no se consiguen nuevos antibióticos capaces hacer frente a las bacterias resistentes. De ahí que este estudio sea esperanzador, en un momento en el que la inversión en la I+D de nuevos antibióticos es insuficiente y en el que no aparecen nuevas móleculas desde hace años.

De la Fuente: “El cuerpo humano es un tesoro de información, un conjunto de datos biológicos”
La labor de César de la Fuente en los últimos años, cuyo objetivo es desarrollar nuevos antibióticos aplicando la informática, le ha valido el Premio Fundación Princesa de Girona de Investigación Científica 2021. En declaraciones recogidas y publicadas en un artículo de la Universidad de Pensilvania, el investigador señala que “el cuerpo humano es un tesoro de información” formado por “un conjunto de datos biológicos”. Explica que “al usar las herramientas adecuadas, podemos buscar respuestas a algunas de las preguntas más desafiantes”.
Y así lo ha hecho. Ha diseñado algoritmos con diferentes parámetros o características fisicoquímicas que tienen en común los péptidos antimicrobianos. Estos algoritmos han buscado e identificado estas moléculas dentro del amplísimo conjunto de proteínas que se expresan en las células humanas. “Aplicamos una nueva forma de usar la inteligencia artificial para descubrir antibióticos en lugares previamente no conocidos”, continúa De la Fuente. “Qué mejor lugar para comenzar que explorar nuestra propia información biológica, la colección de genes y proteínas que nos hacen quienes somos”.
La búsqueda del algoritmo arrojó un resultado de 43.000 péptidos que podían ser posibles antimicrobianos y que se encontraban ocultos en proteínas “más grandes que parecen no tener conexión con el sistema inmunológico” explica el investigador. De hecho, este último es uno de los hallazgos relevantes del estudio: se encontraron péptidos con propiedades antimicrobianas fuera del sistema inmunológico, en otros sistemas como el nervioso, el digestivo o el circulatorio. Por tanto, también pueden tener actividad para hacer frente a las infecciones, más allá del propio sistema inmunológico.
Sintetizaron 55 de estos péptidos antibióticos y los expusieron a ocho patógenos diferentes como bacterias que causan neumonía o la E. coli. El 63,6% mostraron actividad antimicrobiana
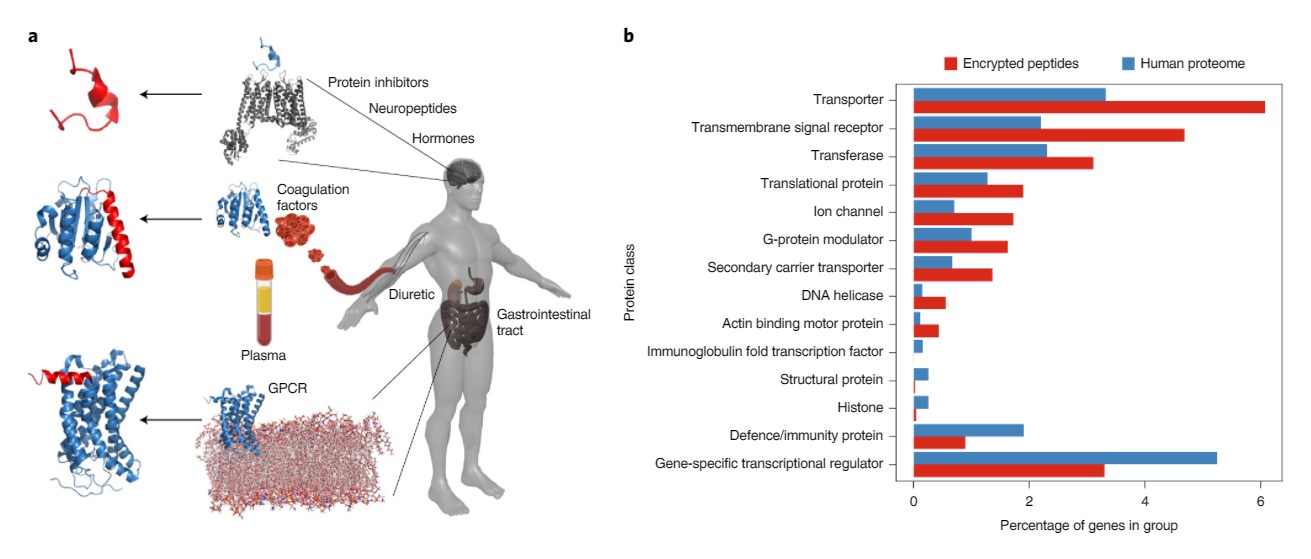
Después de filtrarlos en función de su aptitud, quedaron 2.603. Los investigadores sintetizaron 55 de estos péptidos antibióticos y los expusieron a ocho patógenos diferentes. Entre ellos, bacterias que causan neumonía o la conocida E. coli. Así descubrieron que el 63,6% de los 55 péptidos encriptados mostraban actividad antimicrobina.
Estos péptidos, para sorpresa de los investigadores, también se dirigieron a organismos comensales del intestino y de la piel. “Especulamos que esto podría ser indicativo de un papel modulador de la microbiota que también pueden poseer estos péptidos”, cuenta el líder de la investigación en la web de la Universidad de Pensilvania.
Probaron si estos antibióticos escondidos en proteínas podían actuar de manera sinérgica. El resultado es que podían aumentar su capacidad antimicrobiana 100 veces
También probaron si estos péptidos antibióticos podían actuar de manera sinérgica mezclándolos por su origen en la misma zona biogeográfica del cuerpo. El resultado es que podían aumentar su capacidad antimicrobiana 100 veces. “Es probable que este efecto sinérgico ya esté ocurriendo en nuestros cuerpos”, dice de la Fuente.
Cuando probaron en modelos de ratón, comprobaron que los péptidos se defendían de las infecciones de las bacterias con una capacidad igual que la de antibióticos ya conocidos. Además, no hubo muestra alguna de toxicidad.
La forma en la que atacan a las bacterias, complica la creación de resistencias antimicrobianas
Por último, investigaron sobre posibles resistencias a estos antibióticos naturales. Pero De la Fuente explica que los péptidos encriptados atacan a las bacterias cuando penetran en sus membranas externas, que son básicas para que puedan vivir. “Esta permeación dañina en la membrana requeriría una gran cantidad de energía y múltiples generaciones de mutaciones para crear resistencias en las bacterias. Esto indica que los péptidos son buenos candidatos para antibióticos sostenibles”.
Noticias complementarias:
- Sanidad y Aemps lanzan ‘Antibióticos: tómatelos en serio’, una nueva campaña frente a la resistencia
- Caracterizan la epidemiología y genética de las bacterias intrahospitalarias que provocan nuevas resistencias a antibióticos
- La resistencia a los antibióticos, uno de los mayores retos de la medicina moderna
- El CSIC y el Irycis describen una nueva estrategia para frenar las resistencias a los antibióticos mediante plásmidos
- Resistencias antimicrobianas: El uso de antibióticos en hospitales creció un 40% en la primera ola










