Redacción
UCB recibe el dictamen positivo del CHMP para BIMZELX en el tratamiento de la hidradenitis supurativa

La compañía biofarmacéutica UCB ha recibido la valoración positiva del Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea de Medicamentos (EMA) en el que se recomienda la autorización de bimekizumab para su comercialización en la Unión Europea (UE) como tratamiento para la hidradenitis supurativa (HS) activa de moderada a grave en pacientes adultos con una respuesta inadecuada al tratamiento sistémico convencional.
“El dictamen positivo del CHMP representa un logro significativo para llegar a poner esta nueva opción terapéutica a disposición de las personas que conviven con la hidradenitis supurativa, una enfermedad inflamatoria, crónica y dolorosa de la piel que cuenta con muy pocas opciones de tratamiento”, afirma Emmanuel Caeymaex, vicepresidente ejecutivo de Inmunología y director en Estados Unidos de UCB. “Además, en el caso de recibir la aprobación de la Comisión Europea, se trataría de la cuarta autorización de comercialización para este tratamiento en los últimos tres años y se sumaría a las indicaciones existentes que la terapia ya tiene para la psoriasis en placas de moderada a grave, la artritis psoriásica activa y la espondiloartritis axial activa”, añade.
El Hospital de Bellvitge usa el fármaco esketamina para tratar la depresión resistente
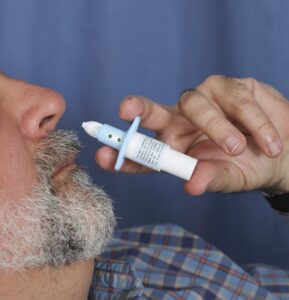
El Hospital Universitari de Bellvitge (HUB) de L’Hospitalet de Llobregat (Barcelona) ha informado este miércoles en un comunicado que ha incorporado el fármaco esketamina en las soluciones terapéuticas para sus pacientes con depresión resistente y ha obtenido resultados “esperanzadores”.
La esketamina es un derivado químico de la ketamina utilizada en anestesia general desde hace décadas y la Agencia Europea del Medicamento (EMA) aprobó en 2022 su uso terapéutico para los casos de depresión resistente en los que han fracasado como mínimo dos líneas de tratamiento antidepresivo.
El paciente se autoadministra el fármaco mediante un espray nasal bajo la supervisión de profesionales médicos y de enfermería en el hospital, donde estará en observación aproximadamente 90 minutos para controlar efectos secundarios transitorios, como el aumento de la presión arterial, nauseas, mareos o episodios leves de disociación.
Pfizer recibe la opinión positiva del CHMP para una nueva combinación Emblaveo infecciones multirresistentes

El Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea del Medicamento (EMA) ha emitido una opinión positiva para aztreonam-avibactam para el tratamiento de pacientes adultos con infección intraabdominal complicada (IIAc), neumonía adquirida en el hospital (NAH), incluida neumonía asociada a ventilación mecánica (NAV), e infección complicada del tracto urinario (ITUc), incluyendo pielonefritis.
“Las bacterias gramnegativas suelen ser resistentes a múltiples fármacos, lo que deja a los pacientes que tienen estas infecciones, muy enfermos y con un alto riesgo de complicaciones graves, incluida la mortalidad”, afirmó José Chaves, director médico de Pfizer en España.
Por ese motivo, añade, “de aprobarse esta combinación podría ofrecer esperanza a los pacientes con infecciones por bacterias gramnegativas potencialmente mortales que actualmente tienen opciones terapéuticas limitadas. Esta recomendación es un paso positivo en la lucha contra las infecciones por bacterias gramnegativas resistentes a casi todos los antibióticos disponibles y demuestra el compromiso de nuestra compañía para hacer frente a la amenaza mundial para la salud pública que supone la resistencia a los antimicrobianos”.
Merck lanza un test de síntomas on line para detectar precozmente el cáncer colorrectal

La compañía Merck ha lanzado un test de síntomas on line como una herramienta de triaje preliminar que lleva a cabo una primera evaluación de los síntomas más comunes relacionados con el cáncer colorrectal en tan solo cinco minutos y, en función de las respuestas e historial, la herramienta te sugerirá los próximos pasos a seguir y, en caso de ser necesario, te remitirá a tu profesional sanitario de referencia.
Además, con motivo del Día Mundial del Cáncer Colorrectal que se celebra este domingo, 31 de marzo, ha compartido el testimonio la oncóloga e investigadora médica, Noelia Tarazona, quien recalca la importancia de los cribados así como de cuidar la alimentación y el estilo de vida, que pueden influir en nuestro riesgo de tener cáncer colorrectal.
“Sí, es una enfermedad que, en muchos casos, da señales que podemos aprender a reconocer: un sangrado inusual en las heces, cambios en los hábitos intestinales, dolores que no desaparecen. Si alguna vez notas algo diferente, por favor, no lo dudes y acude a tu médico de referencia quien sabrá identificar qué está ocurriendo”
Grifols Procleix ArboPlex Assay recibe el marcado CE, el primer y único NAT 4 en 1 para el cribado de arbovirus

Grifols ha anunciado este jueves que su nuevo test Procleix ArboPlex Assay ha obtenido el marcado de Conformidad Europea (CE) con arreglo al Reglamento sobre Diagnóstico In Vitro (IVDR), la primera certificación para una prueba automatizada de ácidos nucleicos (NAT) validada específicamente para cribar donantes de sangre mediante la detección de cuatro importantes arbovirus: los virus del dengue, Zika, chikungunya y del Nilo Occidental.
Estos son los cuatro arbovirus más preocupantes, todos ellos transmitidos por mosquitos vectores. El cambio climático y el aumento de la conectividad mundial han convertido la propagación geográfica de los arbovirus y la gradual exposición a ellos en un importante problema de salud pública. Sólo en el caso del virus del dengue, en 2023 se registraron más de 5 millones de casos y 5.000 muertes en todo el mundo.
“Gracias a su capacidad de detectar cuatro virus en una sola prueba, Procleix ArboPlex Assay puede acelerar y mejorar en general la eficiencia de los laboratorios en el cribado de donantes”, señala Antonio Martínez, presidente de la unidad de negocio Diagnostic de Grifols.
Teva y mAbxience firman un acuerdo estratégico de licencia global para un candidato a biosimilar oncológico

mAbxience, empresa especializada en el desarrollo y fabricación de productos biofarmacéuticos, y parte de los grupos Fresenius Kabi e Insud Pharmas, y Teva Pharmaceuticals International GmbH, una subsidiaria de Teva Pharmaceutical, han anunciado este jueves la firma de un acuerdo estratégico de licencia para un candidato a biosimilar actualmente en desarrollo para el tratamiento de múltiples indicaciones oncológicas. Los biosimilares muestran un potencial prometedor a la hora de proporcionar alternativas más rentables a las terapias oncológicas existentes, abordando así una necesidad crítica en la atención oncológica mundial.
El acuerdo de licencia abarca múltiples mercados mundiales, incluidos Europa y Estados Unidos, lo que supone un gran paso en la estrategia de expansión mundial de mAbxience y respalda un elemento clave de la estrategia Pivot to Growth de Teva, anunciada en 2023, para ampliar su cartera de productos biosimilares mediante el desarrollo empresarial y las asociaciones estratégicas.
Según los términos del acuerdo de licencia, mAbxience aprovechará su experiencia en el desarrollo de biosimilares y sus instalaciones de última generación, con aprobación GMP (Good Manufacturing Practices) en España y Argentina, para desarrollar y producir el producto biosimilar. Teva dirigirá los procesos regulatorios y la comercialización en las regiones designadas, para garantizar el acceso a una población de pacientes más amplia.