Redacción
Los tratamientos de quimioterapia presentan algunos desafíos como la falta de selectividad, que produce efectos secundarios indeseados, y la aparición de quimiorresistencia, que provoca que los tratamientos no sean efectivos en algunos pacientes. Un nuevo estudio publicado en la revista Cell Reports Physical Science ha propuesto el uso de ‘jaulas’ moleculares (formadas por pseudopéptidos) para eliminar células cancerosas de forma selectiva en microambientes ácidos. Para ello, se ha realizado un estudio exhaustivo con una familia amplia de ‘jaulas’ para entender cómo actúan.
El PH ácido que rodea a los tumores sólidos es clave para diferenciar entre células cancerosas y células sanas
Los resultados del trabajo, liderado por un equipo científico del Instituto de Química Avanzada de Cataluña (IQAC-CSIC), del Consejo Superior de Investigaciones Científicas (CSIC), en colaboración con la Universidad de Burgos, son relevantes para el desarrollo preclínico de nuevos ionóforos (moléculas transportadoras de iones) con potencial aplicación terapéutica en el tratamiento contra el cáncer. El estudio también cuenta con la participación del Instituto de Diagnóstico Ambiental y Estudios del Agua (Idaea-CSIC).
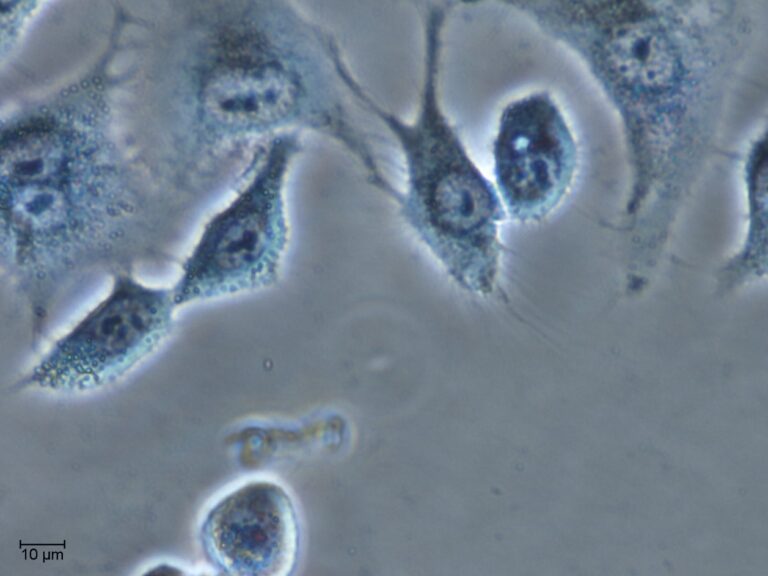
Una de las características de las células de cáncer es que su metabolismo genera un pH ácido en el entorno de los tumores sólidos. Esto confiere unas características especiales a estas células, haciéndolas más resistentes y capaces de migrar a otras zonas del cuerpo (metástasis). El CSIC destaca que hay una evidencia creciente del potencial de los ionóforos como nuevos quimioterapéuticos en cáncer. Sin embargo, el control de su actividad para limitar su toxicidad ha sido una difícil tarea hasta el momento. “El uso de ‘jaulas’ moleculares de este tipo que actúan selectivamente en el pH ligeramente ácido del microambiente de los tumores sólidos es una forma de superar estos obstáculos y avanzar en su desarrollo”, resaltan.
Estas ‘jaulas’ derivadas de aminoácidos sustituidos con flúor matan las células cancerosas en valores de pH ligeramente ácidos (por debajo de 7, que son las cifras observadas alrededor de los tumores), pero son inocuas para el pH fisiológico de los tejidos sanos. “En un estudio previo diseñamos una molécula con estructura tridimensional en forma de ‘jaula’ que mostraba buena selectividad para matar células cancerosas en medios ligeramente ácidos”, explica Ignacio Alfonso, investigador del IQAC-CSIC y autor principal del estudio.
El estudio propone el uso de ‘jaulas moleculares’ que muestran una mayor citotoxicidad en entornos ácidos como los que se encuentran en tumores sólidos
Estas ‘jaulas’ contaban con un átomo de flúor en cada una de las tres cadenas laterales y cuando se encontraba en medios ácidos encapsulaba un cloruro en su interior de manera muy eficiente. Además, era capaz de transportar el cloruro a través de bicapas de lípidos, siendo este transporte también más eficiente cuando había un gradiente de pH con un entorno ácido. Así, resultaba más tóxica para aquellas células que se encuentren en un pH ligeramente ácido como el microentorno de un tumor sólido.
“En este trabajo queríamos ir un poco más lejos y entender el mecanismo de acción de estas moléculas”, explica el investigador del IQAC-CSIC. “Para ello, se ha realizado un estudio exhaustivo con una familia amplia de ‘jaulas’ con diferente número de átomos de flúor en distintas posiciones para entender la capacidad de capturar cloruro, el proceso de transporte y la toxicidad a diferentes pHs en cultivos celulares”, expone Alfonso.
El proceso se ha estudiado exhaustivamente a nivel molecular utilizando enfoques teóricos y experimentales de última generación (fluorescencia, resonancia magnética nuclear y estudios computacionales). Los resultados muestran cuál es el efecto del flúor sobre estas moléculas y, por lo tanto, han permitido entender el mecanismo de acción e identificar una jaula con aún mayor selectividad para matar células de cáncer en entornos ácidos. “Estos resultados ayudarán a comprender y mejorar el diseño de este tipo de ionóforos con potencial aplicación terapéutica en el tratamiento contra el cáncer”, concluye Roberto Quesada, investigador de la Universidad de Burgos.