Redacción
España ya es el país europeo que más ensayos clínicos comerciales inicia. En 2023 adelantó a Alemania, líder hasta ahora en el inicio de estos estudios, según refleja el informe Evaluando el ecosistema de ensayos clínicos en Europa, que ha publicado la consultora Iqvia para Efpia y Vaccines Europe. Este documento destaca el notable papel de España en un contexto de pérdida de competitividad generalizada en el continente frente a potencias como Estados Unidos y China.
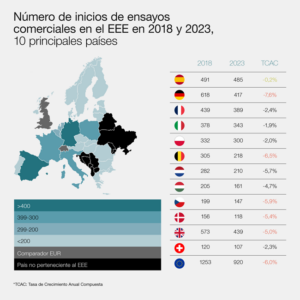
Es cierto que el primer puesto llega más por la fuerte caída en el número de nuevos ensayos en Alemania que por un aumento de estos estudios en España. En 2023 se iniciaron en territorio nacional 485 ensayos mientras que en Alemania lo hicieron 417. Hace cinco años, este país comenzó 618, mientas que España inició 491 (seis más que en 2023).
Entre los factores que han llevado al éxito español, el informe de Iqvia señala la temprana implementación de la regulación europea de ensayos clínicos que España adoptó desde 2016
Según el informe, el éxito español se debe, en gran parte, a la temprana implementación de la regulación europea de ensayos clínicos (CTR), que España adoptó desde 2016. Este marco regulatorio, junto con una infraestructura hospitalaria de alta calidad y un modelo de colaboración eficaz entre ensayos clínicos promovidos por la industria y públicos, ha sido clave para atraer importantes inversiones en investigación clínica. La inversión en este ámbito ha crecido a un ritmo anual del 5,7%, pasando de 479 millones de euros en 2012 a 834 millones en 2022.
El informe también pone en valor la ubicación estratégica de centros de investigación en varias ciudades importantes de España, con más de tres centros de investigación por cada 10.000 kilómetros cuadrados. También destaca el papel del país en el ámbito de los estudios sobre inmunización; excluyendo los años de la pandemia, España inicia una media de 20 ensayos en este ámbito.
El número de ensayos clínicos a nivel mundial aumentó un 38% entre 2013 y 2023, pero en Europa han caído estos estudios 10 puntos porcentuales, del 22% al 12%
A pesar de que el número de ensayos clínicos a nivel mundial ha aumentado un 38% entre 2013 y 2023, Europa ha visto disminuir su porcentaje del 22% al 12%. De hecho, los nuevos ensayos caen en todos los países del Espacio Económico Europeo (EEE) menos en Portugal, Eslovaquia y Grecia. España se ha mantenido con una ligera disminución del 0,2%. Según el documento, esto ha resultado en que 60.000 pacientes europeos hayan perdido la oportunidad de acceder a medicamentos en fase experimental entre 2018 y 2023.
“Los ensayos clínicos europeos se ven obstaculizados por un ecosistema de investigación lento y fragmentado“, señala Nathalie Moll, directora general de Efpia. “Las actuales iniciativas son insuficientes para detener y revertir una década de declive. Para que Europa sea competitiva, debe funcionar como una región unificada y no como Estados Miembros individuales, y estar respaldada por políticas que atraigan inversiones”, añade Moll.
Entre 2013 y 2023 China ha pasado de iniciar el 10% al 42% de los ensayos clínicos en áreas como la oncología, la inmunización, las terapias avanzadas y las enfermedades raras
El informe analiza los ensayos por áreas y se producen caídas similares en oncología, inmunización, enfermedades raras o terapias celulares y génicas, donde la cuota ha descendido del 25 al 10% entre 2013 y 2023. En el mismo período China ha pasado del 10 al 42%, gracias a un entorno regulatorio favorable, financiación y un enfoque estratégico para las terapias avanzadas.
El documento advierte también del declive de los ensayos en pediatría y en los ensayos en fase 1, por su importancia como base para el desarrollo clínico posterior, la inversión y financiación. Por ello subraya que la caída del 19 al 14% en la última década tendrá consecuencias negativas en los próximos años.
En un escenario de declive en nuevos ensayos en el resto del continente, el caso de España ha sido excepcional. Pero desde Farmaindustria advierten de que hay que mucho por hacer para seguir en cabeza. “Los desafíos para mantener la competitividad y reforzar el liderazgo en España son cada vez mayores, y por ello debemos seguir trabajando de forma flexible y colaborativa, anticipándonos a los cambios y con un entorno que nos permita desarrollar la innovación de nuestras compañías”, afirma Amelia Martín Uranga, directora de Investigación Clínica y Traslacional de la patronal de la industria farmacéutica española.
El informe cifra entre 1.000 y 1.500 millones de euros los beneficios para los sistemas sanitarios de la Unión Europea por los pagos por ensayos clínicos y ahorros en costes de medicamentos
El informe subraya la importancia de implementar estrategias para consolidar este liderazgo, como la agilización y simplificación de los procesos burocráticos, la creación de un proceso de fast track para ensayos de fase 1 y la promoción de ensayos clínicos descentralizados. Además, se propone fomentar la investigación en atención primaria y el uso de datos en vida real, con el objetivo de potenciar aún más la capacidad de España para atraer proyectos de investigación y desarrollo en el sector sanitario.
Farmaindustria hace hincapié en que este liderazgo no solo supone un beneficio para la salud de los pacientes, quienes pueden acceder a tratamientos innovadores de manera más temprana, sino también para la economía española. El informe utiliza cifras del Reino Unido para extrapolarlas a la UE y cifra entre 1.000 y 1.500 millones de euros los beneficios para los sistemas por los pagos por ensayos clínicos y ahorros en costes de medicamentos.
Sin embargo, el informe advierte que para que Europa recupere su competitividad a nivel global, es necesario un enfoque más unificado y coordinado. Se aboga por una reforma del Reglamento de Ensayos Clínicos, que permita simplificar y armonizar el proceso de ensayos clínicos en toda la UE, de forma que se faciliten los ensayos multinacionales y se amplíe la capacidad para investigación en el continente.











