..Cristina Cebrián.
Reino Unido apuesta por el principio activo guselkumab, comercializado por Janssen bajo la marca Tremfya. En concreto, el Instituto Nacional para la Salud y la Excelencia en la Asistencia (NICE por sus siglas en inglés) emitió en el mes de mayo una evaluación final positiva, gracias a la cual los adultos que padecen psoriasis en placas de moderada a grave tendrán acceso a este fármaco a través el Servicio Nacional de Salud (NHS) en Inglaterra y Gales. Esta es la primera vez que se atribuye este nivel de beneficio a un tratamiento biológico para la psoriasis.
Los adultos que padecen psoriasis en placas de moderada a grave tendrán acceso a este fármaco a través el Servicio Nacional de Salud (NHS) en Inglaterra y Gales
Por su parte, el organismo de reembolso de fármacos de Alemania, el Comité Federal Conjunto (Gemeinsamer Bundesausschuss; G-BA) publicó también su decisión tras señalar que guselkumab ofrecía “importantes beneficios terapéuticos adicionales” en relación al comparador activo de sus ensayos clínicos (adalimumab), en todas las poblaciones de pacientes evaluadas.
“La rápida decisión por parte de dos de los principales organismos de evaluación de las tecnologías sanitarias de Europa refleja los resultados positivos demostrados en estudios clínicos de guselkumab para el tratamiento de la psoriasis en placas de moderada a grave”, comenta el doctor Jaime Oliver, Medical Lead en Janssen Immunology EMEA.
 Dr. Oliver: “Proporcionar una nueva opción terapéutica podría ayudar a aliviar parte de la carga física y emocional de esta enfermedad”
Dr. Oliver: “Proporcionar una nueva opción terapéutica podría ayudar a aliviar parte de la carga física y emocional de esta enfermedad”
Aliviar las repercusiones psicológicas de la psoriasis
La psoriasis es una enfermedad de la piel que produce descamación en inflamación y, debido a que el proceso de renovación celular de las capas de la piel está acelerado, se desarrollan placas de piel enrojecida bien delimitadas y cubiertas de escamas plateadas. Las placas de psoriasis pueden producir picor y dolor y pueden localizarse en los codos, rodillas, piernas, cuero cabelludo, espalda, cara, genitales, uñas, las palmas de las manos y plantas de los pies.
Además de estos síntomas, se trata de una enfermedad que presenta graves repercusiones psicológicas y proporcionar una nueva opción terapéutica “hace que los pacientes se sientan cohibidos, aislados y deprimidos. Proporcionar una nueva opción terapéutica podría ayudar a aliviar parte de la carga física y emocional de esta enfermedad. Por eso, estamos trabajando de forma intensiva para asegurar que los pacientes elegibles en Europa puedan acceder a guselkumab lo más rápidamente posible”, explica el Dr. Oliver.
Actualmente están en marcha otras evaluaciones de este medicamento en diversos países de la Unión Europea
Estos informes suponen las primeras Evaluaciones de Tecnología Sanitaria (ETS) positivas en Europa para guselkumab después de que recibiera su autorización de comercialización por la Comisión Europea en noviembre de 2017. Actualmente están en marcha otras evaluaciones de este medicamento en diversos países de la Unión Europea y se espera que se emitan las decisiones a lo largo del año.
Control mantenido de la enfermedad
Guselkumab es el primer agente biológico que se dirige selectivamente a la interleuquina (IL)-23, una proteína clave que inicia una respuesta inflamatoria inmunitaria específica en la psoriasis. Otro aspecto positivo que se destaca de las anteriores evaluaciones es que el fármaco puede ofrecer a los pacientes una eficacia favorable y un control mantenido de esta debilitante enfermedad que afecta a aproximadamente 14 millones de personas en toda Europa.
 Guselkumab es un tratamiento inyectable subcutáneo para la psoriasis y los pacientes se lo pueden autoadministrar después de recibir formación. El tratamiento precisa dos dosis de inicio, una inicialmente y la otra cuatro semanas más tarde, seguidas por una dosis de mantenimiento una vez cada ocho semanas en adelante.
Guselkumab es un tratamiento inyectable subcutáneo para la psoriasis y los pacientes se lo pueden autoadministrar después de recibir formación. El tratamiento precisa dos dosis de inicio, una inicialmente y la otra cuatro semanas más tarde, seguidas por una dosis de mantenimiento una vez cada ocho semanas en adelante.
Está en marcha el estudio ECLIPSE de fase III con comparador para evaluar la eficacia de guselkumab frente a secukinumab
Ensayos clínicos en fase III
En cuanto a la investigación, se están llevando a cabo estudios de fase III para evaluar la eficacia y la seguridad de guselkumab en pacientes con artritis psoriásica. Por ejemplo está en marcha el estudio ECLIPSE de fase III con comparador para evaluar la eficacia de guselkumab frente a secukinumab, un inhibidor de IL-17A, en pacientes con psoriasis en placas de moderada a grave.
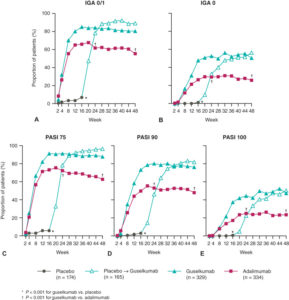
La recomendación del NICE así como el respaldo por el G-BA de guselkumab se basan en datos de estudios clínicos fase III. Los ensayos VOYAGE 1 y 2 compararon guselkumab con placebo y adalimumab, y mostraron niveles elevados de desaparición de las lesiones cutáneas después de 16 semanas, con una puntuación PASI 90 en cerca de 7 de cada 10 pacientes que recibieron guselkumab, en comparación con aproximadamente 5 de cada 10 pacientes que recibieron adalimumab, respectivamente. Algunos datos a largo plazo también demostraron tasas consistentes de desaparición de las lesiones cutáneas en pacientes con psoriasis de moderada a grave que recibieron tratamiento con guselkumab durante casi dos años.