..Redacción.
La Comisión Europea aprueba pembrolizumab como tratamiento de cáncer de pulmón no microcítico (CPNM) metastásico de células escamosas en adultos. Así lo anunció la compañía MSD que comercializa este medicamento bajo la marca Keytruda. Se trata de una terapia anti-PD-1 que, para ser efectiva, se combina con carboplatino y paclitaxel o nab-paclitaxel.
El ensayo fase 3 KEYNOTE-407 mostró una mejora significativa de la supervivencia global (SG) al utilizar esta combinación. El estudio se centra en pacientes adultos con CPNM escamoso metastásico independientemente de su expresión tumoral de PD-L1. Pembrolizumab redujo el riesgo de muerte en un 36%, en comparación con el uso único de quimioterapia. El doctor Luis Paz-Ares, jefe del Servicio de Oncología Médica del Hospital Doce de Octubre de Madrid, comenta esta mejora. “La aprobación supone un hito importante para los pacientes que se enfrentan a este tipo de cáncer difícil de tratar”, comenta.
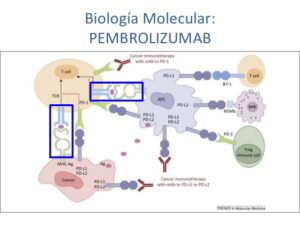 Pembrolizumab redujo el riesgo de muerte en un 36%, en comparación con el uso único de quimioterapia
Pembrolizumab redujo el riesgo de muerte en un 36%, en comparación con el uso único de quimioterapia
El doctor David Vicente, jefe de Sección de la UGC de Oncología Médica del Hospital Virgen Macarena de Sevilla, señala que éste es un estudio pionero. “Es el primero en muchos años que muestra un aumento de supervivencia. Especialmente para los tumores que habían quedado atrás en la evolución de nuevos tratamientos, al carecer de una diana específica”.
La población de especial mal pronóstico se podrá beneficiar de esta combinación de inmunoterapia y quimioterapia, que apenas tenía avances. “La investigación española mantiene una posición muy relevante de la que debemos sentirnos muy orgullosos. La investigación sigue abriendo puertas y añadiendo esperanza a los pacientes con cáncer de pulmón”, apunta el Dr. Vicente.
Tratamiento del cáncer de pulmón en Europa
Con la aprobación de este fármaco se amplían las indicaciones de la combinación en primera línea. “Ahora se puede incluir a pacientes adultos con cáncer de pulmón no microcítico metastásico de tipo escamoso”, explicó Roy Baynes. El responsable médico de MSD Research Laboratories recordó que esta terapia proporciona una base para tratar este cáncer en Europa.
 Dr. Baynes (MSD): “Ahora se puede incluir a pacientes adultos con cáncer de pulmón no microcítico metastásico de tipo escamoso”
Dr. Baynes (MSD): “Ahora se puede incluir a pacientes adultos con cáncer de pulmón no microcítico metastásico de tipo escamoso”
Ahora se amplía la comercialización de la dosis de 200 mg cada tres semanas hasta la progresión de la enfermedad o toxicidad inaceptable. Este principio activo también está aprobado en Europa como tratamiento para otros subtipos de CPNM. Uno de ellos es el que aparece en adultos cuyos tumores no tienen mutaciones de EGFR o ALK. Se comercializa como monoterapia en adultos cuyos tumores tienen elevada expresión de PD-L1 sin mutaciones positivas de EGFR o ALK. También está aprobado en adultos cuyos tumores expresan PD-L1 y que han recibido al menos un régimen de quimioterapia previo.
“Supone un avance significativo puesto que ahora hay un tratamiento de combinación anti-PD-1 aprobado en Europa”, señala el Dr. Baynes. “Hay más pacientes con CPNM que podrían beneficiarse del tratamiento de combinación”, añade.