..Redacción.
La cefalea en racimos episódica cuenta con un nuevo tratamiento inyectable aprobado por la Agencia Americana del Medicamento (FDA). Se trata del anticuerpo monoclonal galcanezumab, comercializado por Lilly bajo la marca Emgality. El fármaco está indicado para tratar la cefalea en racimos episódica en adultos. Su principal novedad es que es el primer y único anticuerpo que se une al CGRP. Este fue aprobado por la FDA para dos tipos distintos de cefaleas.
Christi Shaw (Lilly): “La cefalea en racimos episódica puede ser una enfermedad muy incapacitante y la aprobación de galcanezumab constituye un importante hito”
 “La cefalea en racimos episódica puede ser una enfermedad muy incapacitante. La aprobación de galcanezumab constituye un importante hito, ya que proporciona una nueva opción terapéutica. Ha sido muy esperada por todas aquellas personas que sufren esta patología”, explica Christi Shaw, presidenta de Biomedicinas de Lilly.
“La cefalea en racimos episódica puede ser una enfermedad muy incapacitante. La aprobación de galcanezumab constituye un importante hito, ya que proporciona una nueva opción terapéutica. Ha sido muy esperada por todas aquellas personas que sufren esta patología”, explica Christi Shaw, presidenta de Biomedicinas de Lilly.
Este tipo de cefalea se caracteriza por un inicio abrupto de un dolor de intensidad grave a muy grave en un lado de la cabeza. El dolor se siente en las regiones orbital, supraorbital y/o temporal y puede ir acompañado por síntomas en ese mismo lado del cuerpo. Algunos de ellos son congestión nasal, lagrimeo, miosis o edema palpebral, entre otros. Aunque es una patología muy incapacitante, existe un reto importante a nivel diagnóstico de la enfermedad. Esto se debe a la limitada concienciación que existe. En algunos casos, el diagnóstico puede demorarse de media cinco años o más.
La media de episodios de cefalea en racimos a la semana fue de 17,8 en el grupo de galcanezumab y de 17,3 en el grupo de placebo
Bob Wold, fundador de Clusterbusters, explica su visión como afectado de cefalea en racimos. “Conozco de primera mano la desesperación por lograr nuevas opciones de tratamiento. Para que sean capaces de reducir la frecuencia de unos episodios con un impacto muy incapacitante en nuestras vidas”, comenta.
Reducción de episodios de cefalea en racimos episódica
Para demostrar la eficacia de galcanezumab se desarrolló un ensayo clínico aleatorizado a 8 semanas, doble ciego y controlado con placebo. En el estudio, se aleatorizó a 106 pacientes para que recibieran tratamiento inyectable con galcanezumab 300mg o placebo. Así, la media de episodios de cefalea en racimos a la semana fue de 17,8 en el grupo de galcanezumab y de 17,3 en el grupo de placebo.
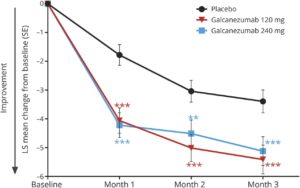 Por otro lado, los pacientes tratados con galcanezumab experimentaron una media de 8,7 episodios menos entre la semana 1 y 3. Mientras que los pacientes en tratamiento con placebo experimentaron 5,2 episodios menos. Además, el 71,4% de los pacientes en tratamiento con galcanezumab vieron sus episodios reducidos a la mitad o más de la mitad en la semana 3. Frente al 52,6% de los pacientes en tratamiento con placebo.
Por otro lado, los pacientes tratados con galcanezumab experimentaron una media de 8,7 episodios menos entre la semana 1 y 3. Mientras que los pacientes en tratamiento con placebo experimentaron 5,2 episodios menos. Además, el 71,4% de los pacientes en tratamiento con galcanezumab vieron sus episodios reducidos a la mitad o más de la mitad en la semana 3. Frente al 52,6% de los pacientes en tratamiento con placebo.
Tan solo dos pacientes en tratamiento doble ciego con galcanezumab tuvieron que abandonar el estudio por efectos secundarios adversos
En cuanto al perfil de seguridad, galcanezumab demostró su consistencia en el ensayo clínico. Tan solo dos pacientes en tratamiento doble ciego con galcanezumab tuvieron que abandonar el estudio por efectos secundarios adversos.
Desde finales de 2018, la Agencia Europa del Medicamento (EMA) y la FDA aprobaron galcanezumab como terapia preventiva de migraña en adultos. Después, en marzo de 2019, recibió la designación de autorización prioritaria en la indicación de prevención de cefalea en racimos. Por la situación acuciante en la que se encuentran estos pacientes. Su uso está contraindicado en aquellas personas con hipersensibilidad grave a galcanezumab a alguno de sus excipientes.










