..Redacción.
Un estudio internacional liderado por el Consejo Superior de Investigaciones Científicas (CSIC) señala que la diabetes constituye un factor de riesgo para desarrollar párkinson. La investigación, publicada en Movement Disorders, explica que la diabetes produce alteraciones a nivel molecular y funcional en los procesos de neurotransmisión de dopamina en las neuronas cerebrales encargadas del control del movimiento, cuya degeneración provoca la enfermedad de Parkinson.
Aunque los análisis epidemiológicos realizados durante varios años apuntaban a que la preexistencia de diabetes puede aumentar el riesgo de padecer párkinson, hasta ahora se desconocían por completo los efectos de la diabetes sobre el cerebro para explicar la asociación de ambas enfermedades. Las neuronas afectadas tienen su somas o cuerpos celulares en una zona del cerebro denominada sustancia negra. Estas proyectan sus prolongaciones o axones al núcleo estriado, una región del cerebro encargada de la función motora y el movimiento del cuerpo.
 Mario Vallejo: “Existe una importante disminución en la expresión de algunas proteínas que regulan la liberación y recaptación de la dopamina en la sinapsis y varicosidades axonales”
Mario Vallejo: “Existe una importante disminución en la expresión de algunas proteínas que regulan la liberación y recaptación de la dopamina en la sinapsis y varicosidades axonales”
“El aumento de los niveles de glucosa en sangre favorece el desarrollo de estrés oxidativo. Este es un efecto adverso posiblemente ligado a la alteración de los niveles de dopamina en el cerebro. También existe una importante disminución en la expresión de algunas proteínas que regulan la liberación y recaptación de la dopamina en la sinapsis y varicosidades axonales”, explica Mario Vallejo, investigador del Instituto de Investigaciones Biomédicas Alberto Sols (IIBM); centro mixto del CSIC y la Universidad Autónoma de Madrid e investigador de Ciberdem, que dirige el proyecto.
Por otro lado, el investigador detalla que la dopamina “normalmente está almacenada dentro de los axones en grupos de vesículas que se abren al exterior y la liberan al espacio interneuronal cuando llega un estímulo eléctrico”. Si esto ocurre, inmediatamente se ponen en marcha mecanismos de compensación que evitan la liberación de una cantidad excesiva del neurotransmisor.
“Es como si, después de pisar el acelerador a fondo, se activara automáticamente un mecanismo que pusiera en marcha un freno o hiciera levantar el pie. Pero en los ratones diabéticos ese freno no funciona bien, debido a la disminución de niveles de un canal de potasio llamado Girk2”, explica Vallejo.
La dopamina que sale al exterior de la neurona en exceso no se recapta bien porque también se alteran dos transportadores de dopamina
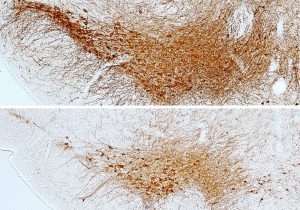 Además, señala que “la dopamina que sale al exterior de la neurona en exceso no se recapta bien porque también se alteran dos transportadores de dopamina. Uno es el encargado de reintroducirla en el axón y el que una vez dentro la almacena en las vesículas. Esto es muy importante porque la dopamina puede ser tóxica en el interior de los axones si no está almacenada en las vesículas. Y es posible que produzca progresivamente daño celular mediante estrés oxidativo”.
Además, señala que “la dopamina que sale al exterior de la neurona en exceso no se recapta bien porque también se alteran dos transportadores de dopamina. Uno es el encargado de reintroducirla en el axón y el que una vez dentro la almacena en las vesículas. Esto es muy importante porque la dopamina puede ser tóxica en el interior de los axones si no está almacenada en las vesículas. Y es posible que produzca progresivamente daño celular mediante estrés oxidativo”.
Colaboración con la Universidad de Oxford
En colaboración con científicos de la Universidad de Oxford, se observó que, en respuesta a un estímulo eléctrico, las neuronas dopaminérgicas de los ratones diabéticos liberan más neurotransmisor que las de los no diabéticos. Así, confirmaron que las alteraciones observadas a nivel molecular afectan a los procesos de neurotransmisión en el núcleo estriado del cerebro.
Aunque los efectos de la diabetes no son suficientes para inducir alteraciones motoras, sí que aumentan la vulnerabilidad de las neuronas dopaminérgicas
Además, aunque los efectos de la diabetes no son suficientes para inducir alteraciones motoras, sí que aumentan la vulnerabilidad de las neuronas dopaminérgicas. De forma que las hacen más sensibles a degenerar por un estímulo nocivo y dar lugar a la aparición de síntomas motores. Curiosamente, estos efectos parecen estar asociados a la hiperglucemia o a la ausencia de señalización por insulina, pero no a la existencia de obesidad. Normalmente esta se relaciona con la diabetes tipo II, el tipo más frecuente en humanos.
Los resultados de la investigación abren nuevas vías de investigación para identificar los mecanismos moleculares por los que la diabetes afecta a los procesos de neurotransmisión en el cerebro. “En los siguientes pasos nos centraremos en analizar si las alteraciones observadas se producen en todo el cerebro; si son consecuencia solo de la presencia de niveles elevados de glucosa o si interviene también el déficit funcional de insulina. Y, finalmente, si pueden prevenirse con algún tratamiento”, concluye Vallejo.