..P.M.
Pfizer y Biontech han anunciado que, tras realizar el análisis final de eficacia en su estudio de fase 3, su vacuna contra el Covid-19 tiene un 95% de eficacia. Su candidata a vacuna Covid-19 basada en ARNm, BNT162b2, cumplió con todos los criterios de valoración principales de eficacia del estudio. Hace unos días informaron que los datos obtenidos a partir del primer análisis de eficacia provisional indicaban una eficacia del 90%.
El análisis de los datos indica esta tasa de eficacia de la vacuna del 95% en participantes sin infección previa por SARS-CoV-2. También en participantes con y sin infección previa por SARS-CoV-2. En ambos casos medido a partir de los siete días posteriores a la segunda dosis.
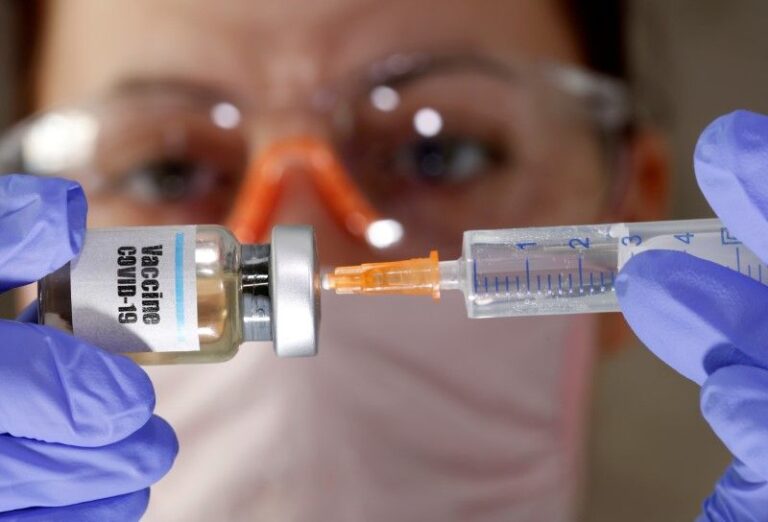
Pfizer y Biontech concluyen los ensayos clínicos de su vacuna contra el Covid-19 con un 95% de eficacia
El análisis de los datos muestra que se evaluaron 170 casos confirmados de Covid-19, de los cuales 162 se observaron en el grupo de placebo frente ocho en el grupo de vacuna. La eficacia fue constante según la edad, el género, la raza y la etnia. Además, la eficacia observada en adultos mayores de 65 años fue superior al 94%. De los diez casos graves observados, nueve se dieron en el grupo de placebo y uno en el grupo vacunado con BNT162b2.
El Comité de Monitoreo de Datos del estudio no ha reportado ningún problema de seguridad serio relacionado con la vacuna. La vacuna fue bien tolerada en todas las poblaciones, con más de 43.000 participantes, y los efectos adversos se resolvieron poco después de la vacunación. Los efectos más importantes de la vacuna fueron fatiga y dolor de cabeza, que afectaron a un 3,8% y un 2% de los voluntarios, respectivamente.
Pfizer ha informado de que se ha logrado el hito de datos de seguridad requerido por la Administración de Drogas y Alimentos de los EE. UU. (FDA) para la Autorización de uso de emergencia (EUA). Por tanto, solicitarán la autorización de su vacuna a la FDA “en unos días“. Asimismo, indican que estos datos se mandarán “a otras agencias reguladoras de todo el mundo“. Pfizer y BioNTech enviarán los datos de eficacia y seguridad para revisión por pares en una revista científica al completar el análisis de los datos.
Pfizer informa que solicitarán la autorización de su vacuna a la FDA “en unos días”
“Los resultados del estudio marcan un paso importante en este histórico viaje de ocho meses para presentar una vacuna capaz de ayudar a poner fin a esta devastadora pandemia. Seguimos avanzando a la velocidad de la ciencia para recopilar todos los datos recopilados hasta ahora y compartirlos con los reguladores de todo el mundo“, señala el Dr. Albert Bourla, presidente y director ejecutivo de Pfizer. “Con cientos de miles de personas en todo el mundo infectadas todos los días, necesitamos urgentemente llevar una vacuna segura y eficaz al mundo“, añade.
Por su parte, Ugur Sahin, MD, CEO y cofundador de BioNTech ha celebrado los resultados del estudio, cuyos datos van a compartir con las autoridades reguladoras. “Nuestro objetivo desde el principio fue diseñar y desarrollar una vacuna que generara una protección rápida y potente contra Covid-19 con un perfil de tolerabilidad benigna en todas las edades. Creemos que lo hemos logrado con nuestra vacuna candidata BNT162b2 en todos los grupos de edad estudiados hasta ahora y esperamos compartir más detalles con las autoridades reguladoras“, indica.
Pfizer y BioNTech esperan producir hasta 50 millones de dosis de vacunas a nivel mundial en 2020 y llegar a las 1.300 millones de dosis para finales de 2021. Pfizer confía en su “dilatada experiencia, conocimientos e infraestructura de cadena de frío existente” para distribuir la vacuna en todo el mundo. Las empresas han desarrollado transportadores térmicos de temperatura controlada especialmente diseñados que utilizan hielo seco para mantener las condiciones de temperatura de -70°C ± 10°C.
Noticias complementarias
- Sanidad autoriza el primer ensayo clínico fase III para la vacuna contra el Covid-19 en España
- La Aemps advierte de la necesidad de regular los medicamentos y vacunas contra el Covid-19
- La vacuna de Moderna contra el Covid-19 muestra una eficacia del 94,5%
- Pfizer y Biontech aseguran una eficacia del 90% en su vacuna contra el Covid-19
- Pfizer espera solicitar a la FDA la autorización para su vacuna del Covid-19 a finales de noviembre