..Redacción.
El 32% de las pacientes con cáncer de mama que sufre una recaída con metástasis presenta un subtipo tumoral diferente del tumor primario. Esto supone cambios en la planificación del tratamiento. Así lo demuestra RegistEM, el primer registro prospectivo con datos de la vida real de pacientes con cáncer de mama avanzado en España.
Este trabajo impulsado por el Grupo GEICAM de Investigación en Cáncer de Mama arroja nuevos resultados que permiten tener mayor conocimiento sobre el tumor, su evolución y respuesta al tratamiento, lo que facilitará su abordaje. RegistEM analiza los datos clínicos, anatomopatológicos y de tratamiento recogidos en la práctica clínica de mujeres con cáncer de mama localmente avanzado no resecable o metastásico. Todas ellas han recaído después de terapia de cáncer de mama localizado o como primer diagnóstico.
RegistEM es el primer registro prospectivo con datos de la vida real de pacientes con cáncer de mama avanzado en España
En la investigación participan 38 hospitales españoles que aportan datos de casi 2.000 pacientes. Los resultados, que fueron presentados en el Congreso de la SEOM, corresponden al análisis de los datos de 485 de las 1.480 mujeres incluidas. Se espera alcanzar las 1.867.
Según los datos recabados, el 34% de las pacientes con cáncer de mama metastásico ya presentaban metástasis desde el diagnóstico. En el 66% restante la metástasis se debe a recaídas tras el tratamiento de un tumor localizado.
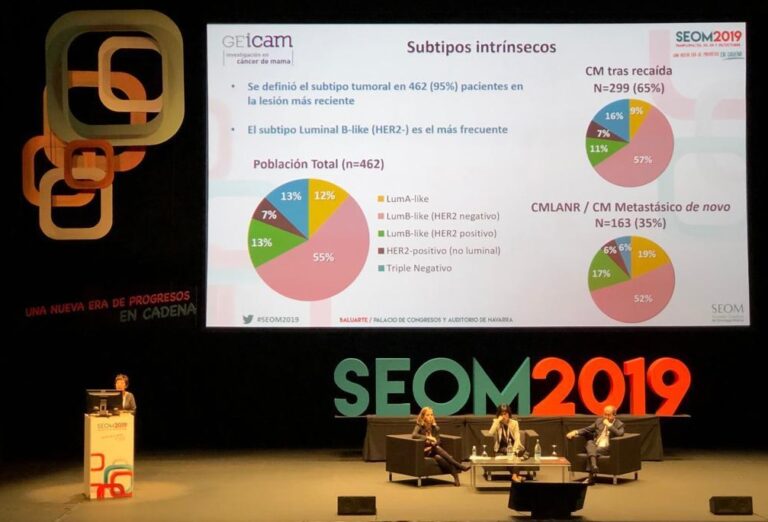
El análisis también concluye que el subtipo más frecuente (en las 462 mujeres donde se detecta subtipo tumoral) es el Luminal B (HER2- negativo), que lo padecen el 55% de pacientes. Le siguen el Luminal B (HER2-positivo) y el triple negativo, ambos con el 13%; y por último, el Luminal A (12%) y el HER2-enriquecido (7%).
El estudio también analiza si se produce un cambio del subtipo de cáncer desde el tumor primario a la metástasis. Esto ocurre en el 32% de las mujeres. El cambio más frecuente es de Luminal A a Luminal B(HER2-negativo). Esta información “abre la posibilidad a poder utilizar fármacos muy útiles como terapia anti-HER2 u hormonoterapia en pacientes en las que, por los hallazgos del análisis inmunohistoquímico esto no se consideró indicado en su momento“, apunta el doctor Carlos Jara, jefe de la Unidad de Oncología del Hospital Universitario Fundación Alcorcón – Universidad Rey Juan Carlos de Madrid y vocal de la Junta Directiva de GEICAM.
El cambio más frecuente en la evolución del tumor primario a las metástasis es el de Luminal A a Luminal B HER2 negativo
También se deduce que el 93% de pacientes que modifican el subtipo reciben un tratamiento adecuado al subtipo de la lesión metastásica. Y es que el estudio también ofrece información sobre las terapias utilizadas, siendo la más frecuente los taxanos, un tipo de quimioterapia. Además, el estudio analiza las localizaciones de las lesiones metastásicas, siendo el hueso la más frecuente (59%), especialmente en subtipos luminales.
Al 39% de las pacientes se les practica una biopsia de la lesión metastásica, sobre todo del hígado y los ganglios linfáticos. La realización de la biopsia depende de la abordabilidad de la estructura anatómica donde se halla la metástasis. “Una localización como la piel o los ganglios linfáticos, así como el hígado, puede considerarse relativamente accesible; en cambio, las metástasis óseas son algo más complicadas en su abordaje para biopsia y otras como las del sistema nervioso deben considerarse virtualmente inaccesibles de modo rutinario”, explica el doctor Jara.
“Las valoraciones moleculares sobre las muestras de las pacientes posibilitarán abrir nuevas vías de desarrollo terapéutico”, afirma el especialista. Toda la información recogida va a “permitir mejorar en el abordaje de estos pacientes”, explica Isabel Álvarez, médico adjunto de la Sección de Oncología Médica del Hospital Universitario de Donostia, coordinadora del grupo de trabajo de la enfermedad HER2 y vocal de la Junta directiva del Grupo GEICAM.
Toda la información recogida en la investigación de Grupo GEICAM va a permitir mejorar en el abordaje de estos pacientes
La doctora Álvarez, además, señaló que, “como grupo de investigación, GEICAM va a mejorar los ensayos clínicos y programas de investigación en estas pacientes“. Este estudio ha generado un gran interés. De hecho, se presentaron cinco posters en relación a este trabajo y una comunicación oral en el último Congreso de la Sociedad Española de Oncología Médica (SEOM).
RegistEM cuenta con representación de pacientes con todos los subtipos de cáncer de mama y que hayan sido diagnosticados de enfermedad avanzada durante los años 2016 y 2019. Se les hará un seguimiento durante al menos cinco años desde la inclusión del último paciente.
El cáncer de mama avanzado continúa siendo una enfermedad incurable, con una media de supervivencia de tres años y una supervivencia a los cinco años del 25%. Se considera que no es una sola patología sino varias, en función del subtipo de tumor que se padezca, y tener uno u otro condiciona la forma de manejar la enfermedad desde el punto de vista terapéutico.
Por otra parte, también se presentó en el Congreso SEOM2019 otra investigación del Grupo GEICAM. Según este trabajo, el índice neutrófilo/linfocito (INL) se presenta como un marcador de inflamación y de respuesta del sistema inmunitario frente al cáncer. Se basan en datos recogidos de los estudios ETNA (Evaluating Treatment with Neoadyuvant Abraxane) y GEICAM/2006-03.
Niveles elevados del marcador de inflamación INL parecen asociarse con peor respuesta al tratamiento en tumores triples negativos
Los resultados confirman que niveles elevados de este índice, antes y sobre todo tras el tratamiento con quimioterapia neoadyuvante, parecen asociarse con peor respuesta al tratamiento en tumores con subtipo triple negativo. “Aunque habría que confirmarlo en estudios prospectivos, estos resultados podrían estar indicando los pacientes que van a responder menos a la terapia y que, por lo tanto, van a tener peor pronóstico“, subraya uno de los coordinadores del estudio, el doctor Alberto Ocaña.
Otro de los estudios de Grupo GEICAM presentados durante el Congreso SEOM2019 como comunicación oral es una parte de los subestudios traslacionales del ensayo PANGEA-breast. Concretamente, la que trata de determinar el papel de las células mieloides supresoras (del inglés MDSC) que forman parte del sistema inmune y que parecen ejercer un efecto inmunosupresor muy potente mediante una variedad de mecanismos de acción cada vez mejor conocidos.
Una investigación de Grupo GEICAM el papel de las células mieloides supresoras (MDSC) y si podrían identificarse como un biomarcador inmune
La detección de MDSC en tejido y sangre periférica podría aportar importante información de pronóstico sobre este cáncer e incluso servir para monitorizar la enfermedad y la repuesta a los tratamientos. Según los datos presentados, el nivel de MDSC se encuentra elevado en pacientes con cáncer de mama frente a una población sana. Además, parece que, en las mujeres en las que se obtienen resultados satisfactorios con la terapia aplicada, estas células disminuyen de manera notable. Incluso, se elevan cuando se detecta progresión de enfermedad.
Los resultado pueden identificar las MDSC como un biomarcador inmune. Otra de las preguntas sobre las que trabajan es si estas células son causa o consecuencia del cáncer de mama, al menos, en etapas avanzadas. “Si fuese lo primero, estaríamos ante una diana terapéutica de primera magnitud”, asegura el Dr. Luis de la Cruz, jefe del Servicio de Oncología Médica del Hospital Universitario Virgen Macarena de Sevilla y vocal del del Grupo GEICAM.
Por otra parte, este grupo de investigación presentó un estudio sobre las alteraciones de las copias genómicas como predictor de la respuesta a la terapia neoadyuvante en cáncer de mama localizado.
Entre los principales resultados, destaca que el tratamiento neoadyuvante en cáncer de mama localizado modifica el genoma del tumor. Además, la erradicación del tumor tras tratamiento neoadyuvante (RCp) se asocia con las modificaciones genéticas. La investigación ha identificado que seis genes del cromosoma 21 (CHAF1B, CBR3, CBR1, RCAN1, SLC5A3 y RUNX1) están relacionados con la eficacia del tratamiento.
Identificados estos seis genes, el paso siguiente es validarlos en una población más amplia de pacientes para determinar si están relacionados con una RCp. “Si es así, podremos identificar en qué pacientes es efectiva la quimioterapia como terapia neoadyuvante y en cuáles no”, explica el doctor Federico Rojo, responsable de Patología del Hospital Universitario Jiménez Díaz de Madrid, coordinador del grupo de trabajo TransGEICAM y vocal de la Junta Directiva del Grupo GEICAM.
Noticias relacionadas:
- Dra. Ana Lluch: el 85% de los casos de cáncer de mama tienen curación
- FECMA y Novartis elaboran un decálogo reclamando mayor esfuerzo en investigación y concienciación contra el cáncer de mama
- Dr. García Foncillas: “Tenemos los primeros datos de beneficio clínico en cáncer de mama triple negativo con inmunoterapia”
- El cáncer de mama no conoce fronteras ni colores
- La industria farmacéutica lidera en España cerca del 90% de los ensayos clínicos en tumores de mama