..Cristina Cebrián.
A día de hoy, el glioblastoma es el tumor cerebral primario maligno más agresivo y frecuente en el adulto. Las investigaciones sobre esta enfermedad se encaminan a poder controlar la enfermedad y mejorar su pronóstico. Para ello, la búsqueda de un biomarcador del glioblastoma puede ser clave. Un estudio de la Clínica Universidad de Navarra (CUN) busca biomarcadores sanguíneos del glioblastoma, como método diagnóstico menos invasivo y que permita desarrollar nuevas estrategias que faciliten su diagnóstico.
El coordinador del Área de Neuro-oncología de la CUN, el Dr. Jaime Gállego, quien lidera el estudio, explica a iSanidad la importancia de contar con un biomarcador del glioblastoma en un medio más accesible como es la sangre.
¿Qué supone para la práctica clínica encontrar un biomarcador sanguíneo del glioblastoma?
Un biomarcador en si mismo puede tener diferentes utilidades. Por ejemplo, de diagnóstico de la enfermedad, utilidad pronóstica que nos permita saber cómo va a evolucionar la enfermedad en el paciente y utilidad de predicción de respuesta a los tratamientos. Con estas funcionalidades, en glioblastoma ya existen algunos biomarcadores, pero la mayoría requieren el estudio de tejido tumoral. Son biomarcadores moleculares que se obtienen del estudio de la propia pieza tumoral obtenida mediante cirugía. También existen biomarcadores de imagen, sobre todo de resonancia magnética.
Sería muy útil encontrar unas moléculas que podamos hallar fácilmente mediante una extracción sanguínea y que nos diesen información diagnóstica o pronóstica del glioblastoma
 Para la práctica clínica sería un gran avance encontrar un biomarcador con estas funcionalidades en un medio más accesible como es la sangre. Es decir, encontrar unas moléculas que podamos hallar fácilmente mediante una extracción sanguínea y que nos diesen información diagnóstica o pronóstica, o también que nos permita monitorizar la enfermedad. Todo esto sería muy interesante, porque simplificaría mucho el manejo y seguimiento de los pacientes.
Para la práctica clínica sería un gran avance encontrar un biomarcador con estas funcionalidades en un medio más accesible como es la sangre. Es decir, encontrar unas moléculas que podamos hallar fácilmente mediante una extracción sanguínea y que nos diesen información diagnóstica o pronóstica, o también que nos permita monitorizar la enfermedad. Todo esto sería muy interesante, porque simplificaría mucho el manejo y seguimiento de los pacientes.
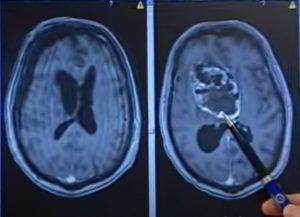
Hay que tener en cuenta que para diagnosticar a estos pacientes se tienen que someter a cirugía y, después, el seguimiento clínico se hace mediante resonancias magnéticas cerebrales de forma muy periódica. De modo que, encontrar una molécula en la sangre que nos permita simplificar este seguimiento sería de gran utilidad.
¿Puede ayudar a facilitar el diagnóstico y aplicar tratamientos personalizados a los pacientes?
Es cierto que encontrar un biomarcador diagnóstico en glioblastoma sería de gran utilidad, pero no hay que olvidar que la cirugía es necesaria en esta patología tumoral. Es un pilar fundamental del tratamiento. Por tanto, en la mayoría de casos, tener un biomarcador diagnóstico no va a evitar realizar después una cirugía. Si esto es así, al final el diagnóstico lo vamos a tener mediante el estudio de la muestra extirpada quirúrgicamente.
En pacientes que no son candidatos a cirugía sería especialmente útil un biomarcador diagnóstico de glioblastoma para descartar otras enfermedades cerebrales sin tener que llegar a la cirugía
La utilidad de un biomarcador diagnóstico sí puede ser muy útil en aquellos pacientes que no son candidatos a cirugía, bien por la localización de la lesión, o bien por encontrarse muy deteriorados clínicamente y tener mucha comorbilidad. En este sentido si que sería especialmente útil un biomarcador diagnóstico de glioblastoma para descartar otras enfermedades cerebrales sin tener que llegar a la cirugía.
 Otra utilidad importante es que facilita monitorizar la evolución de la enfermedad. Cuando un paciente se opera y se trata con terapia estándar de radioterapia y quimioterapia, hay que vigilar que el tratamiento está funcionando. Esto lo hacemos evaluando clínicamente al paciente y con resonancias magnéticas cada dos o tres meses. A veces la resonancia nos muestra una imagen con la que no sabemos si el tumor está creciendo o es una reacción inflamatoria causada por los tratamientos. Por tanto, tener un marcador en sangre que nos permita ver la evolución de la enfermedad sin necesidad de recurrir frecuentemente a las resonancias sería muy útil.
Otra utilidad importante es que facilita monitorizar la evolución de la enfermedad. Cuando un paciente se opera y se trata con terapia estándar de radioterapia y quimioterapia, hay que vigilar que el tratamiento está funcionando. Esto lo hacemos evaluando clínicamente al paciente y con resonancias magnéticas cada dos o tres meses. A veces la resonancia nos muestra una imagen con la que no sabemos si el tumor está creciendo o es una reacción inflamatoria causada por los tratamientos. Por tanto, tener un marcador en sangre que nos permita ver la evolución de la enfermedad sin necesidad de recurrir frecuentemente a las resonancias sería muy útil.
Aún así esto, a día de hoy, es muy hipotético e idealista. Todavía no disponemos de biomarcadores sanguíneos fiables que nos permitan evaluar la respuesta al tratamiento y monitorizar la enfermedad. Es un campo de investigación que está por desarrollar ampliamente.
La incidencia aproximada cada año es de entre 3 y 5 casos por cada 100.000 habitantes. Es una enfermedad poco frecuente pero extremadamente relevante por su gravedad
En su investigación hablan de las microvesículas de células tumorales en sangre, ¿qué función tienen exactamente?
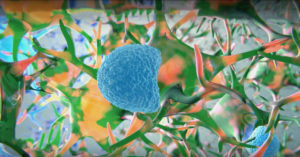
Son vesículas muy pequeñas que liberan todas las células del organismo y es un medio de comunicación intercelular. Es decir, las células se comunican entre si liberando sustancias y también vesículas. Es como si una célula manda un paquete con un contenido a otra célula receptora que lo utilizará para diferentes funciones.
Se ha demostrado que las células tumorales tienen mayor capacidad de secretar vesículas que las células normales. Son células mucho más activas. Estas microvesículas contienen material genético, proteínas o moléculas de la propia célula tumoral. Ese contenido que se excreta en estas microvesículas tiene otras células receptoras. El objetivo de esas microvesículas, en el caso de los tumores, es facilitar la proliferación de las células tumorales y aumentar la invasividad del tumor. También facilitan la diseminación a distancia o la metástasis. Incluso pueden contribuir a frenar la respuesta inmune propia del organismo frente al tumor.
El glioblastoma es el tumor cerebral primario maligno más agresivo y frecuente en el adulto, ¿cuál es su incidencia en España y en el mundo?
Dentro de los gliomas, el tumor más frecuente y agresivo es el glioblastoma. No deja de ser una enfermedad rara por su incidencia y prevalencia global. Los estudios de incidencia a los que más hacemos referencia son los que se realizan en Estados Unidos. En la población europea y en España se asume que la incidencia es muy similar a estos registros estadounidenses. En este sentido, la incidencia aproximada cada año es de entre 3 y 5 casos por cada 100.000 habitantes. Es una enfermedad poco frecuente pero extremadamente relevante por su gravedad.
Hay que acabar con el nihilismo terapéutico. Tenemos que actuar porque, aunque no curemos la enfermedad, cada vez tratamos mejor a los pacientes con esta enfermedad
¿Cuál es el pronóstico de este tipo de tumor cerebral?
Es una enfermedad que tiene un pronóstico muy sombrío, por ser el tumor cerebral primario maligno más agresivo y frecuente. A día de hoy, es una enfermedad que no somos capaces de curar. Pero, frente a esto, hay que acabar con el nihilismo terapéutico. Tenemos que actuar porque, aunque no curemos la enfermedad, cada vez tratamos mejor a los pacientes con esta enfermedad.
Por otro lado, yo nunca hablo de estadísticas en un paciente, porque sirven para tener una idea general. Pero hablar de una estadística en una persona es lo primero que podemos hacer para equivocarnos.
Hay factores que determinan una evolución más favorable o desfavorable de cada paciente. Por ejemplo, influyen factores pronósticos clínicos como la edad. De hecho, cuanto más joven es el paciente, mejor pronóstico habrá. El estado funcional es otro factor, ya que no es lo mismo una persona que está muy discapacitada a otra que está en pleno estado físico y neurológico. También influye el grado de extirpación del tumor y de la recepción quirúrgica de la lesión. La mezcla de estos factores clínicos y moleculares determinan, en cierta manera, el pronóstico.
Si logramos controlar durante mucho tiempo la enfermedad, quizá en el futuro vayan saliendo nuevas alternativas terapéuticas.
La idea que yo trato de transmitir al paciente, sabiendo la crudeza de la enfermedad, es dar pie a la esperanza. Siempre hay pacientes que responden al tratamiento, aunque no quiere decir que se vayan a curar, pero si se les puede controlar la enfermedad durante el mayor tiempo posible. Esto a veces lo conseguimos, por lo que los clínicos tenemos que luchar como si fuese el paciente que responde al tratamiento. Si logramos controlar durante mucho tiempo la enfermedad, quizá en el futuro vayan saliendo nuevas alternativas terapéuticas.
¿Hacia dónde se dirigen los nuevos tratamientos para el glioblastoma, ¿qué papel tiene la inmunoterapia en este tipo de tumor?
Este es uno de los tumores en los que quizá se han producido menos avances. A día de hoy, el tratamiento estándar consiste en la combinación de cirugía y radioterapia y quimioterapia. Este tratamiento se utiliza desde 2005. Tambien se han hecho ensayos clínicos para tratar de encontrar otros tratamientos que mejoren los resultados del tratamiento estándar. Pero, a día de hoy, no se ha conseguido.
Esto no quiere decir que estemos igual que hace 15 años. Yo diría que con el mismo tratamiento de hace 15 años conseguimos mejores resultados, porque cada vez conocemos mejor la enfermedad. Y cada vez conocemos mejor cómo aplicar estos tratamientos, además de perfeccionar más la cirugía y la radioterapia. También sabemos secuenciar más otras opciones terapéuticas si la enfermedad avanza. Por tanto, los avances tecnológicos nos han permitido, con el mismo tratamiento, mejorar el pronóstico de los pacientes que sufren glioblastoma.
Los avances tecnológicos nos han permitido, con el mismo tratamiento, mejorar el pronóstico de los pacientes que sufren glioblastoma
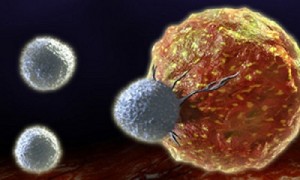 Sobre hacia dónde se dirigen, ha habido mucha investigación sobre terapias diana aunque ninguna de estas ha demostrado con firmeza un beneficio claro. Otra línea de investigación es la inmunoterapia, que en este campo se desarrolla más lentamente que en otros tumores, por la particularidad que tiene el tumor y el órgano que lo aloja que es el cerebro. Este es un órgano de difícil acceso y este tumor genera una coraza que le protege de la respuesta inmune.
Sobre hacia dónde se dirigen, ha habido mucha investigación sobre terapias diana aunque ninguna de estas ha demostrado con firmeza un beneficio claro. Otra línea de investigación es la inmunoterapia, que en este campo se desarrolla más lentamente que en otros tumores, por la particularidad que tiene el tumor y el órgano que lo aloja que es el cerebro. Este es un órgano de difícil acceso y este tumor genera una coraza que le protege de la respuesta inmune.
De modo que se están intentando desarrollar diferentes técnicas de inmunoterapia para tratar de controlar la enfermedad. Por ejemplo, fármacos inhibidores de la evasión del sistema inmune, vacunas con células dendítricas o la aplicación de infusión de virus oncolíticos dentro del propio tumor. Se están desarrollando diferentes estrategias de inmunoterapia pero, a día de hoy, todavía no se han convertido en un tratamiento estándar.
Aquí es todavía más importante el tópico de que no hay enfermedades sino enfermos. Probablemente no haya glioblastomas, sino que cada glioblastoma tiene unas características particulares. Tenemos que identificar qué pacientes con glioblastoma responden a un tratamiento y qué pacientes no lo hacen. Ahí es donde tenemos que dar el siguiente paso, tratar de ir a la enfermedad de cada paciente.
Ojalá consigamos controlar muy bien localmente la enfermedad, para poder actuar después a distancia. En cualquier caso, bienvenidos sean todos los tratamientos locales que permitan mejorar el pronóstico de los pacientes
También se está investigando un nuevo abordaje farmacológico basado en la terapia fotodinámica para el tratamiento de los gliomas de alto grado, ¿cree que puede resultar efectivo?
Esta terapia consiste en aplicar al paciente una sustancia o fármaco fotosensibilizador. Esa sustancia se va a quedar adherida a la célula tumoral y, cuando se aplica una luz sobre la célula tumoral, se genera una reacción química entre la sustancia y el haz de luz que produce la muerte celular.
Esto se está intentando desarrollar desde hace tiempo y puede ser una línea de investigación muy útil porque hay radiosensibilizadores y se pueden aplicar haces de luz. Lo que ocurre es que este haz de luz se tiene que aplicar en el gesto quirúrgico muy probablemente, ya que la bóveda craneal nos impide el paso del haz de luz.
Aunque en el futuro puede resultar muy beneficioso, una de las desventajas es que no deja de ser un tratamiento local, como ocurre con la cirugía y la radioterapia. El glioblastoma no es una enfermedad local, sino que es una enfermedad del cerebro. Entonces, el problema puede ser que la enfermedad aparezca por otro lado del cerebro al que no ha llegado esa terapia. Ojalá consigamos controlar primero muy bien localmente la enfermedad, para poder actuar después a distancia. En cualquier caso, bienvenidos sean todos los tratamientos locales que permitan mejorar un poco el pronóstico de los pacientes.
Noticias complementarias
- La Clínica de Navarra prueba una nueva terapia combinada de virus e inmunoterapia en pacientes con tumor cerebral
- El Hospital Clínic, el Idibaps y Gebro Pharma firman un acuerdo para desarrollar terapias contra el glioblastoma
- Tan solo el 5% de pacientes con glioblastoma vive cinco años después del diagnóstico










