..Redacción.
Los pacientes de cáncer de pulmón no microcítico (CPNM) positivo para la quinasa del linfoma anaplásico (ALK+) disponen ya de una nueva opción terapéutica. Brigatinib (Alunbrig) ha recibido el visto bueno del Ministerio de Sanidad como tratamiento de primera línea. Así lo ha confirmado la compañía farmacéutica Takeda en una rueda de prensa junto a los doctores Mariano Provencio, presidente del Grupo Español de Cáncer de Pulmón (GECP) y jefe del servicio de Oncología Médica del Hospital Universitario Puerta de Hierro de Majadahonda (Madrid), y Rosario García Campelo, jefa del Servicio de Oncología del Complejo Hospitalario Universitario A Coruña (CHUAC).
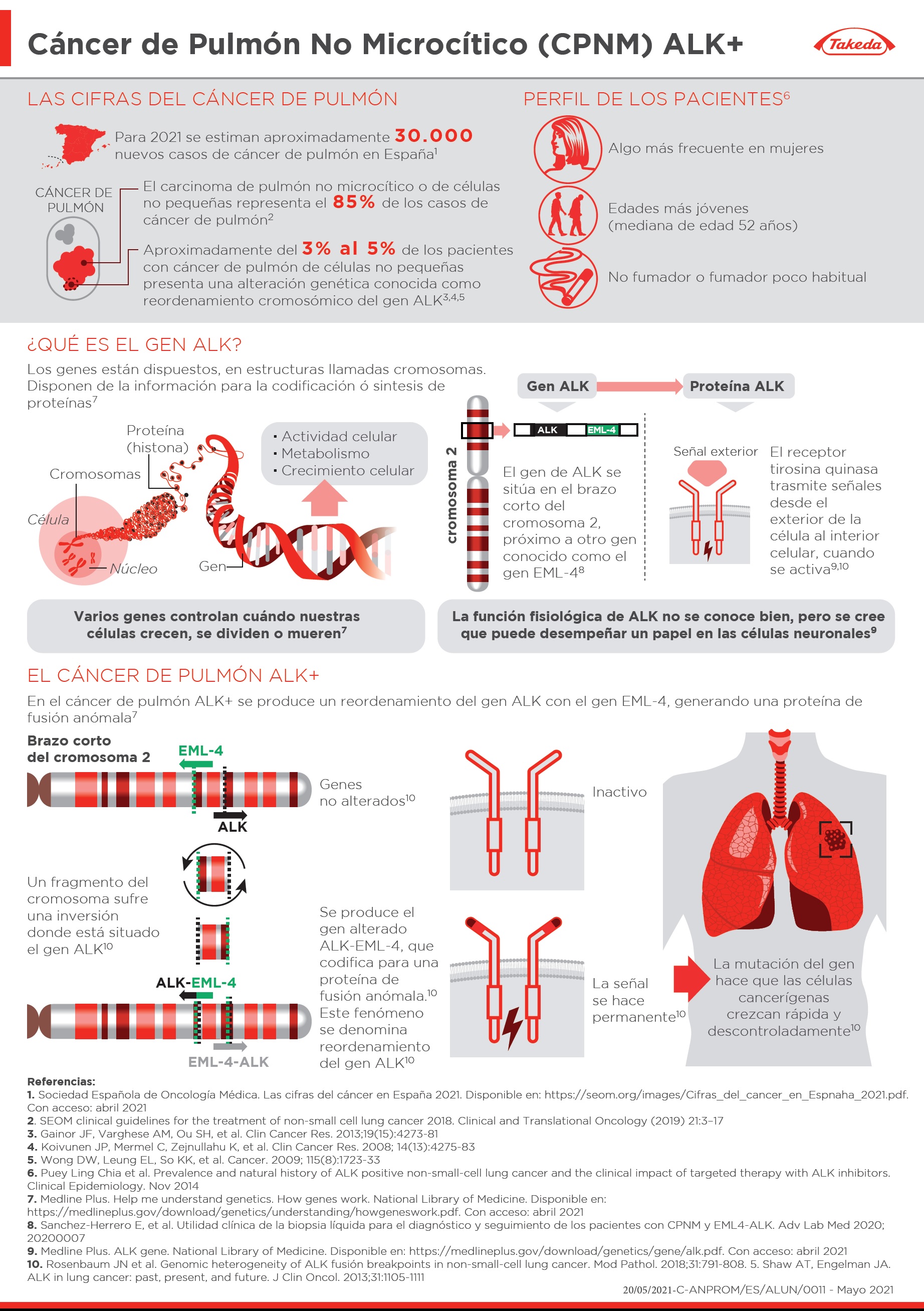
El reordenamiento de ALK está presente en aproximadamente un 5% de los tumores de pulmón no microcítico. Aunque su incidencia es baja, tiene un gran impacto en la supervivencia y en la calidad de quienes lo padecen. El perfil más frecuente mujer con una mediana de edad de 52 años y en personas que no fuman o fuman poco. Además, un 60% de los pacientes con este tipo de tumor, que suele detectarse en estadios avanzados, acaban desarrollando metástasis cerebrales. Precisamente por el diagnóstico en fases avanzadas, un 40% debuta ya con una metástasis cerebral.
Brigatinib (Alunbrig) ha recibido el visto bueno del Ministerio de Sanidad como tratamiento de primera línea frente a cáncer de pulmón no microcítico ALK+
“Gracias al mayor conocimiento que tenemos de estos tumores en la última década sabemos que no estamos tratando con una única enfermedad, sino con una auténtica constelación de subenfermedades con alteraciones moleculares específicas”, destaca el Dr. Provencio.
La Dra. García Campelo destacó el cáncer de pulmón no microcítico como un paradigma en la medicina de precisión. “Un claro reflejo de los avances en medicina de precisión es que, para los pacientes con CPNM avanzado portadores de la traslocación de ALK, se dispone hoy de un amplio arsenal terapéutico con inhibidores de ALK (ALKi) de segunda generación que han demostrado una potente actividad en primera línea en comparación con crizotinib, tanto en términos de eficacia sistémica como de eficacia cerebral”, añadió la especialista.
Un total de 13 hospitales del Sistema Nacional de salud han participado en los ensayos clínicos para el desarrollo de este medicamento. Se trata de una terapia dirigida -inhibidor de la tirosina-quinasa (TKI) de segunda generación- diseñada para inhibir ALK, el oncogén C-ROS 1 (ROS1) y el receptor 1 del factor insulínico de crecimiento (IGF-1R, por sus siglas en inglés), además de superar mecanismos de resistencia asociados a otros inhibidores ALK.
Los ensayos clínicos, de dos años de seguimiento, han revelado que esta nueva opción terapéutica demostró un eficacia sistémica e intracraneal superior a crizotinib, reduciendo el riesgo de progresión intracraneal o de muerte en un 69% en los pacientes con metástasis cerebrales de inicio. De hecho, según los resultados de los ensayos clínicos, los pacientes tratados con este nuevo medicamento vivieron más del doble de tiempo sin que la enfermedad progresara que aquellos pacientes que recibieron el tratamiento estándar. “Nos vamos a 24 meses frente a los 11 cuando el paciente recibe el tratamiento convencional”, destacó la Dra. García Campelo.
Noticias complementarias:
- La Comisión Europea aprueba brigatinib, como tratamiento de primera línea en cáncer de pulmón no microcítico ALK+
- Takeda inicia el desarrollo de un tratamiento derivado del plasma para el Covid-19
- ‘Hemofilia y tú’, una página web de Takeda para pacientes con coagulopatías congénitas y adquiridas
- Takeda se suma a las asociaciones de pacientes para cambiar la percepción de la palabra raro