..G.M.
Es uno de los misterios de la investigación en cáncer: cómo las células cancerosas, en algunos casos, permanecen inactivas durante años después de separarse del tumor primario y llegar a otras partes del cuerpo y cómo es el proceso por el que “despiertan” y desarrollan las metástasis.
Han descubierto que las células tumorales diseminadas que causan las metástasis secretan colágeno tipo III que las mantiene inactivas
Las investigaciones de un equipo de científicos del Instituto de Cáncer Tisch en Monte Sinaí (Nueva York), liderado por el investigador español José Javier Bravo-Cordero, han descubierto que estas células tumorales diseminadas modifican su entorno, es decir, remodelan la matriz extracelular formando un nicho que enriquecen con colágeno tipo III que las propias células derivadas del tumor secretan y que las mantiene “dormidas”.
Es cuando el nivel de este colágeno disminuye, cuando las células cancerígenas se reactivan y forman las metástasis. Con estos hallazgos, los investigadores probaron a enriquecer el entorno de las células cancerígenas en ratones con este colágeno y vieron que se interrumpió la progresión del cáncer. El trabajo realizado por este grupo de científicos se publicó este lunes en la revista Nature Cancer.
Es cuando el nivel de este colágeno disminuye, cuando las células cancerígenas se reactivan y forman las metástasis
 Según explica el Dr. José Javier Bravo-Cordero, investigador principal del estudio, estos hallazgos “tienen implicaciones clínicas potenciales y pueden conducir a un biomarcador novedoso para predecir la recurrencia de tumores”. Pero los resultados de la investigación pueden abrir la puerta para ir un paso más allá hacia “una intervención terapéutica para reducir las recaídas locales y distantes”.
Según explica el Dr. José Javier Bravo-Cordero, investigador principal del estudio, estos hallazgos “tienen implicaciones clínicas potenciales y pueden conducir a un biomarcador novedoso para predecir la recurrencia de tumores”. Pero los resultados de la investigación pueden abrir la puerta para ir un paso más allá hacia “una intervención terapéutica para reducir las recaídas locales y distantes”.
Otras investigaciones habían descrito cómo las células tumorales dispersas salen del estado de latencia, pero este estudio enseña cómo las células están inactivas. Un aspecto clave para pensar en estrategias terapéuticas para prevenir la metástasis. “A medida que se descubre la biología de la latencia tumoral y se desarrollan nuevos fármacos específicos, una combinación de tratamientos que inducen la latencia con terapias que se dirigen específicamente a las células inactivas evitará en última instancia la recurrencia local y la metástasis y allanará el camino hacia la remisión del cáncer”, explica el Dr. Bravo-Cordero.
Dr. Bravo-Cordero: “Nuestros hallazgos tienen implicaciones clínicas potenciales”
La microscopía de dos fotones de segunda generación permitió al equipo observar las células cancerosas dormidas en tiempo real y en un animal vivo. Concretamente en ratones que habían tenido tumores de mama y de cabeza y cuello. Los investigadores rastrearon las células turmorales, vieron cómo se volvían inactivas creando esos nichos con colágeno. Después, pudieron observar el proceso de cambio en la matriz extracelular en el paso de latencia a reactivación. En este proceso comprobando que se producían alteraciones en la arquitectura y en la abundancia del colágeno tipo III.
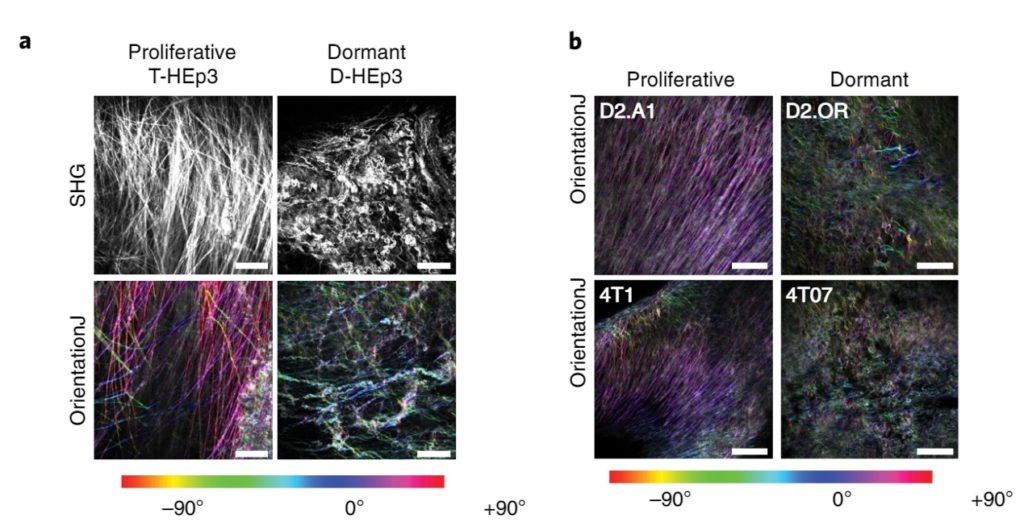
Cuando los científicos aumentaron la cantidad de colágeno tipo III en el entorno de las células cancerosas dispersas, estas volvieron a inactivarse. Como consecuencia de esa inactividad se detuvo la progresión del cáncer. Además, los investigadores demostraron en muestras de pacientes que “una gran cantidad de colágeno podría usarse como una medida potencial para predecir la recurrencia del tumor y la metástasis”, señala el Instituto de Cáncer Tisch.
Los científicos aumentaron la cantidad de colágeno tipo III en el entorno de las células cancerosas, que volvieron a inactivarse. La consecuencia fue que se detuvo la progresión del cáncer en ratones
“Nuestros datos apoyan la idea de que la manipulación de estos mecanismos podría servir como una barrera para la metástasis a través de la inducción de la inactividad de las células tumorales diseminadas”, concluyen los autores del estudio.
Noticias complementarias:
- Investigadores del CNIO descubren un mecanismo involucrado en los primeros momentos de la metástasis del melanoma
- Hallan cómo el ácido palmítico promueve la metástasis y deja una memoria más agresiva en las células tumorales
- Investigadores descubren un nuevo lugar donde se esconden las células madre del cáncer de mama para formar la metástasis
- El equipo del Dr. Massagué descubre que las células cancerígenas inician la metástasis sirviéndose de la capacidad para curar heridas
- Investigadores españoles hallan características inmunes comunes en las metástasis del cáncer de pulmón