..Cristina Cebrián.
El Servicio de Oftalmología del Hospital 12 de Octubre de Madrid ha administrado la primera terapia génica aprobada en España para el tratamiento de un tipo de distrofia hereditaria de la retina que afecta a niños y adultos jóvenes. En concreto, se trata de la producida por la mutación del gen RPE65. Este hospital es uno de los cuatro centros españoles y el único de la región madrileña designado para el uso del fármaco voretigén neparvovec, desarrollado por Novartis y comercializado como Luxturna. La Dra. Pilar Tejada, jefa de Sección de Oftalmología del Hospital 12 de Octubre, comenta con iSanidad los resultados a corto plazo que ofrece esta terapia y la mejora en la calidad de vida de estos pacientes.
¿En qué consiste esta terapia génica aprobada para tratar distrofia hereditaria de la retina producida por la mutación del gen RPE65?
Esta es la primera y única terapia aprobada, a día de hoy, para un grupo concreto de distrofias hereditarias de la retina: aquellas que presentan mutaciones en el gen RPE65.
Dentro de este grupo de enfermedades con esta mutación hay distintas expresiones clínicas. Las más importante es la amaurosis congénita de Leber, que se presenta desde los primeros momentos de la vida. De hecho, es la forma más temprana y más severa de todas las distrofias de retina. También es la responsable de los casos de ceguera en la primera década de la vida. Además, hay otras formas clínicas que tienen esta mutación, como las distrofias retinianas graves que se inician en etapas tempranas de la vida y, en algunos casos, la retinosis pigmentaria.
Esta terapia génica es importante porque, además de ser la primera que actúa sobre la causa de la enfermedad, es una terapia génica de reemplazo del gen enfermo por uno sano
 El gen RPE65 codifica la proteína RPE65, encargada de realizar el ciclo visual. Es decir, transforma la luz que llega a la retina (fotón) en una señal eléctrica. En este grupo de enfermedades, al producirse la mutación del gen, la consecuencia es que no se produce esta proteína y, por tanto, no se genera el ciclo visual. Con el tiempo, se va produciendo la muerte de las células retinianas.
El gen RPE65 codifica la proteína RPE65, encargada de realizar el ciclo visual. Es decir, transforma la luz que llega a la retina (fotón) en una señal eléctrica. En este grupo de enfermedades, al producirse la mutación del gen, la consecuencia es que no se produce esta proteína y, por tanto, no se genera el ciclo visual. Con el tiempo, se va produciendo la muerte de las células retinianas.
Esta terapia génica es importante porque, además de ser la primera que actúa sobre la causa de la enfermedad, es una terapia génica de reemplazo del gen enfermo por uno sano. En concreto, se introduce un gen sano en un vector que, en este caso, es un virus adenoasociado que actúa como transporte del gen. Así, se mete bajo la retina con el fin de que este virus infecte con el gen RPE65 sano a las células sanas de la retina, que ya son capaces de producir la proteína encargada del ciclo visual. Para poder aplicar este tratamiento es muy importante que existan células sanas que no se hayan visto afectadas por la enfermedad.
¿Qué complejidades presenta la aplicación de este tratamiento?
No hay que olvidar que esta terapia consiste en una cirugía compleja del ojo, la vitrectomía. El cirujano de retina elimina el gel vítreo y tiene que introducir el medicamento debajo de la retina a partir de un pequeño agujero. Para ello, realiza un desprendimiento de retina.
Lo ideal sería que, en un futuro, estos medicamentos de terapia génica se puedan introducir con una inyección intraocular, como ya se hace con las degeneraciones maculares
En el caso de los niños, se trata de una cirugía muy compleja porque el gel vítreo que rellena el globo ocular está muy adherido a la retina y hay que liberarlo. Lo ideal sería que, en un futuro, estos medicamentos de terapia génica se puedan introducir con una inyección intraocular, como ya se hace con las degeneraciones maculares.
¿Cuál es la forma clínica de presentación de la amaurosis congénita de Leber?
Estos pacientes ya muestran clínica desde el nacimiento, aunque a veces se tarda en diagnosticar por desconocimiento de los padres e incluso de los oftalmólogos. Son niños que no fijan la vista, están como ausentes, sin esa comunicación visual propia de la edad y, a veces presentan nistagmos, les vibran los ojos muy rápido.
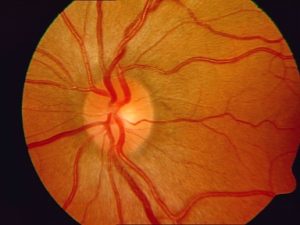 Otra característica de esta patología es la foto adicción. Es decir, se quedan extasiados con los focos de luz. Por todo ello, suele aparecer un retraso madurativo del que a veces tarda en definirse la causa. Los pacientes tienen dificultades tremendas para manejarse en ambientes con poca iluminación y esto ya se ve desde las primeras etapas de la vida. Además, es algo progresivo porque cada vez van necesitando más iluminación para hacer su vida normal.
Otra característica de esta patología es la foto adicción. Es decir, se quedan extasiados con los focos de luz. Por todo ello, suele aparecer un retraso madurativo del que a veces tarda en definirse la causa. Los pacientes tienen dificultades tremendas para manejarse en ambientes con poca iluminación y esto ya se ve desde las primeras etapas de la vida. Además, es algo progresivo porque cada vez van necesitando más iluminación para hacer su vida normal.
Se trata de una enfermedad que conduce a la ceguera, por lo que si no se actúa la ceguera está asegurada en etapas tempranas de la vida. Por tanto, frenar la evolución de la enfermedad es ya un hito histórico
Por otro lado, se produce una pérdida del campo visual periférico y se reduce hasta quedar restos visuales centrales. Asimismo, esta enfermedad también afecta a la visión central y se produce una pérdida progresiva de la visión. De hecho, puede llegarse a una ceguera completa en edad juvenil.
¿Qué resultados a corto plazo ofrece esta terapia génica?
Aunque el fármaco no puede revertirlo todo, porque las células muertas no se pueden recuperar, se ha visto en ensayos clínicos que frena la progresión de la enfermedad. Esto es algo importantísimo porque se trata de una enfermedad que conduce a la ceguera, por lo que si no se actúa la ceguera está asegurada en etapas tempranas de la vida. Por tanto, frenar la evolución de la enfermedad es ya un hito histórico.
En términos de agudeza visual y de campo visual, las mejorías se constatan poco, pero el mayor beneficio es la capacidad de los pacientes para manejarse mejor en ambientes poco iluminados. Esto les permite caminar, deambular y manejarse con mayor autonomía. En definitiva, esto repercute positivamente en su calidad de vida.
En nuestro Servicio hemos trabajado mucho en categorizar muy bien a los pacientes y hacer una valoración mediante pruebas que no era obligatorio hacerlas en los protocolos
 ¿Qué criterios siguen a la hora de seleccionar a los pacientes candidatos a recibir este tratamiento?
¿Qué criterios siguen a la hora de seleccionar a los pacientes candidatos a recibir este tratamiento?
Deben ser pacientes con un diagnóstico de distrofia hereditaria de la retina con mutación del gen RPE65. En este sentido, es importante que la comprobación genética de esta mutación se haya hecho en un laboratorio certificado y que se constate que es bialélico (alelo paterno y alelo materno).
Otro criterio de selección es que los niños deben ser mayores de tres años, porque se trata de una cirugía muy compleja, aunque lo ideal sería hacerlo cuanto antes. Este es el límite de edad que se ha considerado para que los riesgos de la cirugía no sean tan extremos. Además, los pacientes deben tener un tejido retiniano viable. Es decir, contar con células sanas que puedan infectarse por el virus.
Una vez aplicado el tratamiento, ¿cuál es el seguimiento a los pacientes?
Nos preocupa muchísimo cómo vamos a valorar los cambios después del tratamiento. Por eso, en nuestro Servicio hemos trabajado mucho en categorizar muy bien a los pacientes y hacer una valoración mediante pruebas que no era obligatorio hacerlas en los protocolos. Hemos aportado nuestra experiencia en exploración funcional de niños y la hemos aplicado a esta patología.
La idea es que tengamos información sobre los desafíos de la vida real a los que se enfrentan estos pacientes, al mes, a los tres meses y con cierta periodicidad
Lo que nos interesa es ser capaces luego de valorar. Por ejemplo, si se van a producir muchos cambios con respecto al campo visual y a la agudeza visual. También si se van a producir cambios en las pruebas que hagamos de tomografía para medir la retina. En definitiva, hemos construido un circuito que es el mismo que se utilizó en el ensayo clínico sobre Luxturna y que lo aprobó la Agencia Americana del Medicamento (FDA), aunque en España no se ha incluido.
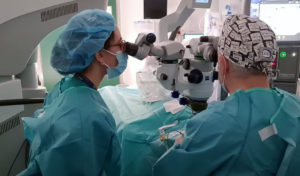 Se trata de una habitación con obstáculos y la luz se regula con diferentes niveles. Creemos que es importante que el paciente recorra este circuito complejo antes y después del tratamiento para poder hacernos una idea de cómo se maneja. Si el paciente es capaz de recorrer este circuito y superar los obstáculos con diferentes niveles de luz, esto supondrá un cambio positivo.
Se trata de una habitación con obstáculos y la luz se regula con diferentes niveles. Creemos que es importante que el paciente recorra este circuito complejo antes y después del tratamiento para poder hacernos una idea de cómo se maneja. Si el paciente es capaz de recorrer este circuito y superar los obstáculos con diferentes niveles de luz, esto supondrá un cambio positivo.
Es una forma objetiva de calibrar si el paciente ha mejorado o no después del tratamiento. También elaboramos encuestas de calidad de vida en edad pediátrica. La idea es que tengamos información sobre los desafíos de la vida real a los que se enfrentan estos pacientes, al mes, a los tres meses y con cierta periodicidad.
No conocemos el número exacto de pacientes que presentan esta mutación del gen, porque quizá están infra diagnosticados
¿A cuántos pacientes podría beneficiar el tratamiento?
Existe una base de datos muy importante que pertenece a la Fundación Jiménez Díaz y agradezco a la Dra. Carmen Ayuso su contribución al diagnóstico de esta enfermedad. Ellos han sido los que han diagnosticado a estos pacientes desde el punto de vista genético.
No conocemos el número exacto de pacientes que presentan esta mutación del gen, porque quizá están infra diagnosticados. Pero, en nuestro caso, ya hemos operado a dos pacientes y tenemos a otros cinco pacientes que han superado la evaluación del Comité de Selección de Terapias Avanzadas de la Comunidad de Madrid. También están entrando pacientes nuevos a estudio.
Para aplicar este tipo de terapia en su hospital, ¿han realizado algún tipo de formación específica?
Los retinólogos están acostumbrados a realizar esta cirugía de retina, no es algo nuevo para ellos. Lo que es nuevo es la introducción de ese fármaco concreto. Pero, aún así, han recibido una formación específica por parte de Novartis y cuentan con la acreditación para realizar esta cirugía.
Noticias complementarias
- Dr. Héctor de la Riva: «Las terapias génicas están cambiando el paradigma en las distrofias hereditarias de retina»
- Alex Sanfeliú (Novartis): “Las terapias génicas en oftalmología traerán esperanza a pacientes que no tenían alternativas terapéuticas”
- La industria intensifica su apuesta por las enfermedades raras: de ocho tratamientos en 200 a 169 hoy