..Redacción.
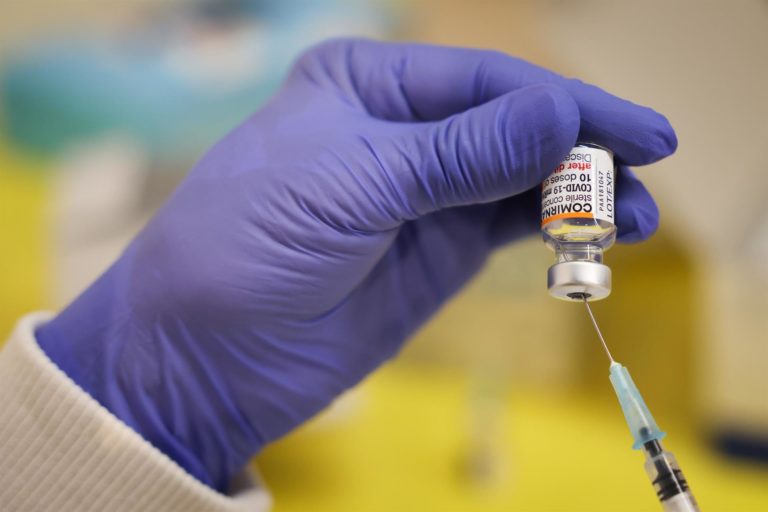
La farmacéutica Pfizer y su socio BioNTech han solicitado a la Administración de Alimentos y Medicamentos de Estados Unidos la autorización de su vacuna de refuerzo Covid-19 reformulada, dirigida a dos subvariantes de ómicron que están en amplia circulación.
La vacuna de refuerzo se ha modificado para las subvariantes ómicron BA.4 y BA.5 para personas de 12 años o más. Las dos compañías esperan que la solicitud correspondiente a la Agencia Europea del Medicamento se complete también en los próximos días. A la espera de la autorización, las dosis estarán disponibles para su envío inmediato, añaden. Todavía no hay un ensayo clínico para la versión BA.4/BA.5 del refuerzo.
Ambas compañías esperan que la solicitud correspondiente a la Agencia Europea del Medicamento se complete también en los próximos días
Las empresas anunciaron previamente los datos de seguridad y tolerabilidad de los ensayos de fase 2 y 3 de una dosis de refuerzo de 30 microgramos de su vacuna candidata BA.1-adaptada, que combina la vacuna existente y una vacuna dirigida a la variante de la proteína Ómicron BA.1.
Así, la vacuna bivalente adaptada a Ómicron BA.1 provocó una respuesta inmunitaria superior contra la variante BA.1 en comparación con la actual vacuna Covid-19. Pero la BA.1 ha sido desplazada desde entonces por otras subvariantes en los últimos meses. Este hecho ha provocado la necesidad de nuevas reformulaciones.
Noticias complementarias
- La vacuna española, más cerca: Hipra espera la autorización de la EMA para sacar 250 millones de dosis
- Un estudio apunta que las vacunas de ARNm contra el Covid-19 son seguras en pacientes con insuficiencia cardíaca
- El daño pulmonar persiste un año después de sufrir neumonía por Covid, según un estudio
- Un estudio señala que el 66% de los positivos por Covid-19 continúa infectando cinco días después de los síntomas
- La incidencia en mayores baja de 200 casos y la ocupación hospitalaria se sitúa por debajo del 4%