..Redacción.
Tralokinumab ha obtenido la recomendación del Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea del Medicamento (EMA) para ampliar su indicación a pacientes adolescentes de 12 a 17 años que padezcan dermatitis atópica de moderada a grave y que sean candidatos a tratamiento sistémico. El fármaco está comercializado por LEO Pharma con el nombre de Adtralza.
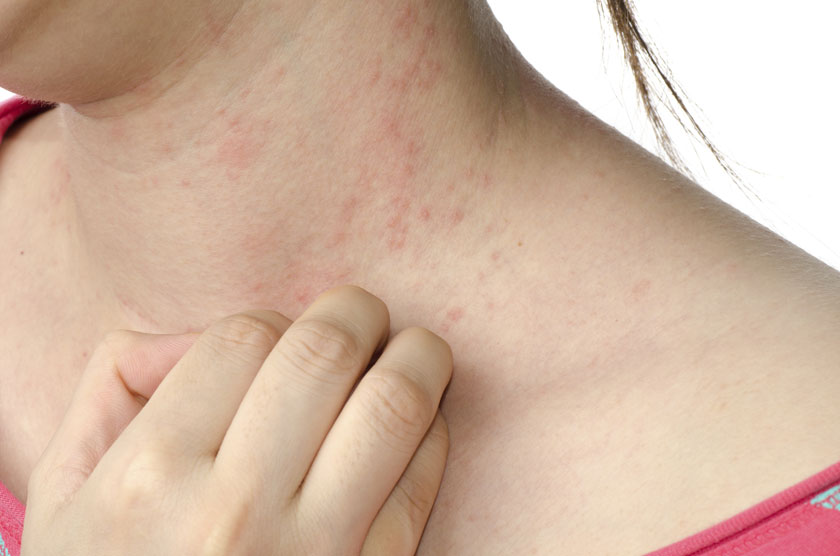
Hasta el momento, el anticuerpo monoclonal humano tralokinumab se había aprobado para tratar la dermatitis atópica en adultos, ahora puede llegar a los adolescentes
Hasta el momento, este anticuerpo monoclonal humano se había aprobado para tratar la dermatitis atópica en adultos. Con el visto bueno de la EMA para que la Comisión Europea conceda la autorización del uso del medicamento en este grupo de edad, Europa se convertirá en el primer mercado en diponer de tralokinumab para tratar a adolecentes.
La dosis recomendada para los pacientes adolescentes es de 600 mg al inicio seguida de 300 mg cada dos semanas. Se trata de la misma dosis que para los pacientes adultos. La opinión positiva de la EMA se basa en los datos del ensayo de fase 3 Ecztra 6. El estudio evaluó tralokinumab en monoterapia en comparación con un placebo en este grupo de pacientes adolescentes.
Christophe Bourdon: “Existen opciones de tratamiento limitadas para los adolescentes en la UE que viven con dermatitis atópica de moderada a grave”
“Existen opciones de tratamiento limitadas para los adolescentes en la UE que viven con dermatitis atópica de moderada a grave. A través de nuestros esfuerzos clínicos, hemos trabajado para garantizar que haya suficientes datos para respaldar la comercialización de una nueva opción biológica para estos pacientes”, ha dicho Christophe Bourdon, director ejecutivo de LEO Pharma. “La opinión del CHMP subraya nuestra confianza en el perfil de seguridad y la eficacia de este anticuerpo mientras buscamos obtener la aprobación regulatoria para expandir su indicación de uso en la población de pacientes adolescentes”, ha añadido.
Valoraron la puntuación de la Evaluación Global del Investigador de aclaramiento total o casi total (IGA 0/1) y una mejora de al menos un 75% en la puntuación del Índice de Gravedad y Área del Eccema (EASI-75). También valoraron la extensión y gravedad de la dermatitis atópica, una mejora de al menos 4 puntos en la puntuación media semanal en la Escala Numérica del Peor Prurito Diario (NRS) de los adolescentes y la puntuación del índice de Calidad de Vida en Dermatología para Niños (CDLQI).
Noticias complementarias
- Dr. Kozarzewski: «La llegada de tralokinumab cambia la vida de pacientes que llevan toda su vidas con dermatitis atópica»
- La prestación farmacéutica incluye tralokinumab para la dermatitis atópica de moderada a grave en adultos
- Más de un tercio de los adultos con dermatitis atópica tiene dificultades para lidiar con los síntomas de la enfermedad
- LEO Pharma y LTS comienzan un ensayo clínico de parches de microagujas para tratar la psoriasis