Redacción
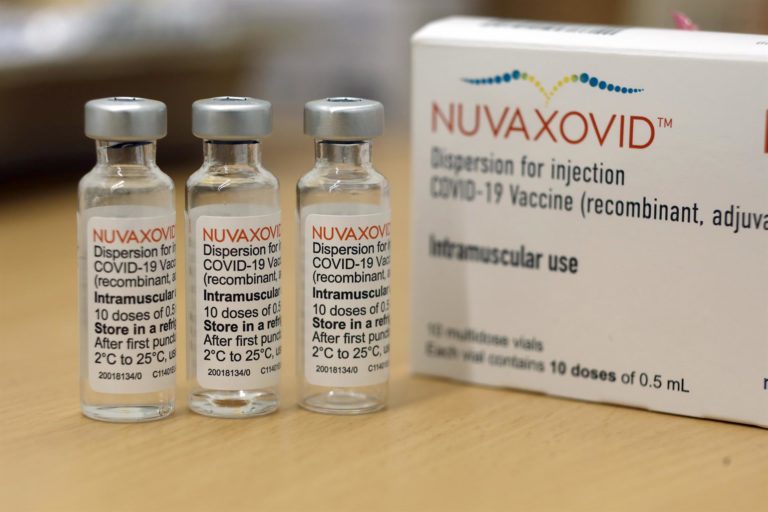
Novavax ha anunciado que la Organización Mundial de la Salud (OMS) ha ampliado el uso de emergencia de su vacuna contra el Covid-19 como serie primaria de dos dosis en adolescentes de 12 a 17 años y como refuerzo en adultos de 18 años o más.
“La actualización nos permite ofrecer nuestra vacuna basada en proteínas como serie primaria para adolescentes y como refuerzo para adultos en todo el mundo. Los países miembros de la OMS cuentan ahora con una opción de vacuna para estas indicaciones desarrollada con un enfoque innovador de la tecnología tradicional. Además, esta vacuna puede almacenarse en refrigeración estándar, lo que facilita su transporte”, ha comentado el presidente y director ejecutivo de Novavax, Stanley C. Erck.
En concreto, la OMS ha avalado la vacuna de Novavax como serie primaria en adolescentes de 12 a 17 años, gracias los datos de la ampliación pediátrica en curso del ensayo de fase 3 ‘PREVENT-19’. En la investigación participaron 2.232 adolescentes de 12 a 17 años de 75 centros de Estados Unidos. La ampliación pediátrica, la vacuna alcanzó su objetivo principal de eficacia. Asimismo, demostró una eficacia clínica global del 80% en un momento en el que la variante Delta era predominante en Estados Unidos.
La vacuna alcanzó su objetivo principal de eficacia y demostró una eficacia clínica global del 80%
Los datos preliminares de seguridad de la expansión pediátrica mostraron que la vacuna fue generalmente bien tolerada. Los acontecimientos adversos graves y severos fueron escasos en número y equilibrados entre los grupos de vacuna y placebo. No se consideró que los acontecimientos estuvieran relacionados con la vacuna. Las reacciones adversas más comunes observadas fueron dolor en el lugar de la inyección, dolor de cabeza, mialgia, fatiga y malestar. No hubo un aumento de la reactogenicidad en los adolescentes más jóvenes en comparación con los adolescentes mayores. Tampoco se observó ninguna nueva señal de seguridad en la parte controlada con placebo de la ampliación pediátrica.
En cuanto a su uso como dosis de refuerzo en adultos, este aval se debe a los datos del ensayo de fase 2 de Novavax realizado en Australia, de otro ensayo de fase 2 realizado en Sudáfrica y del ensayo COV-Boost patrocinado por el Reino Unido. Como parte de los ensayos de fase 2 de Novavax, se administró una dosis única de refuerzo de la vacuna a participantes adultos sanos aproximadamente seis meses después de su serie de vacunación primaria de dos dosis de la misma vacuna.
La tercera dosis produjo un aumento de la respuesta inmunitaria comparable o superior a los niveles asociados a la protección en los ensayos clínicos de fase 3. En el ensayo ‘COV-Boosy’, la vacuna de Novavax indujo una respuesta significativa de anticuerpos cuando se utilizó como tercera dosis heteróloga de refuerzo.