Redacción
La Comisión Europea ha aprobado dupilumab en la Unión Europea (UE) para tratar la dermatitis atópica grave en niños de seis meses a cinco años que son candidatos para el tratamiento sistémico. De esta forma, dupilumab -que se está desarrollando por Sanofi y Regeneron- se convierte en el primer y único medicamento indicado para tratar a estos niños tanto en Europa como en EE.UU.
“Ver a un bebé o a un niño pequeño lidiar con los efectos debilitantes y de gran alcance de una dermatitis atópica grave es desgarrador. He sido testigo personalmente de cómo esta enfermedad crónica de la piel puede alterar las vidas de familias enteras cuando no se controla. Intervenir con tratamientos eficaces durante la lactancia y la primera infancia puede ayudar a controlar el impacto desafiante que esta enfermedad tiene en los niños y sus familias durante estos años de formación”, declara la Dra. Korey Capozza, fundadora y directora ejecutiva de Global Parents for Eczema Research (GPER).
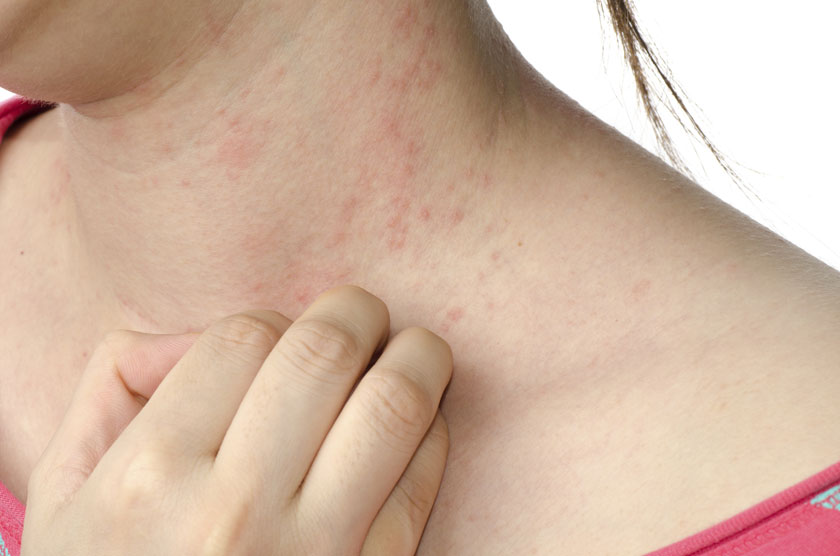
La dermatitis atópica es una enfermedad crónica derivada de la inflamación tipo 2. Entre el 85% y el 90% de los pacientes desarrollan síntomas por primera vez antes de los cinco años de edad, que a menudo puede continuar hasta la edad adulta. Los síntomas incluyen picor intenso y persistente, y lesiones cutáneas que cubren gran parte del cuerpo, lo que provoca sequedad cutánea, agrietamiento, dolor, enrojecimiento u oscurecimiento, costras y exudado, y todo esto puede aumentar el riesgo de infección cutánea. La dermatitis atópica grave también puede afectar significativamente a la calidad de vida de los niños pequeños y de sus familias. Las opciones de tratamiento actuales en este grupo de edad son principalmente corticoesteroides tópicos, que pueden asociarse a riesgos de seguridad y afectar al crecimiento cuando se utilizan a largo plazo.
Los pacientes tratados con dupilumab experimentaron una rápida reducción del picor tres semanas después de haber empezado el tratamiento y apreciaron mejoras significativas a las 16 semanas que se mantuvieron durante un año
Según el Dr. Naimish Patel, jefe de Desarrollo Global, Inmunología e Inflamación de Sanofi, “una gran mayoría de las personas con dermatitis atópica comienzan a desarrollar síntomas durante sus primeros años de vida, los más vulnerables, y estos síntomas a menudo pueden continuar durante el resto de sus vidas. Con esta última aprobación, Dupixent es el primer medicamento biológico para personas que viven con dermatitis atópica desde la infancia hasta la edad adulta. Dado que su perfil de seguridad y eficacia está bien establecido, Dupixent tiene el potencial de transformar el panorama para personas de todas las edades que viven con dermatitis atópica. Seguimos comprometidos a explorar Dupixent para el tratamiento de otras enfermedades cutáneas inflamatorias crónicas”.
Para el Dr. George D. Yancopoulos, presidente y director científico de Regeneron, “ningún bebé o niño debería pasar sus primeros días sufriendo el picor intenso e implacable y el dolor cutáneo de la dermatitis atópica. Con demasiada frecuencia, los padres y cuidadores de niños con dermatitis atópica grave se desesperan por recibir nuevos tratamientos para tratar esta enfermedad crónica. En el ensayo pivotal, Dupixent redujo el picor y el dolor cutáneo y mejoró la calidad de vida relacionada con la salud y la calidad del sueño. Dupixent se ha recetado a más de medio millón de pacientes de todo el mundo en todas las indicaciones aprobadas. Esta última aprobación de la UE aporta la eficacia probada y, lo que es más importante, el perfil de seguridad a largo plazo de Dupixent a esta población especialmente vulnerable”.
Se trata de la tercera aprobación de Dupixent que realiza la Comisión Europea en los últimos tres meses
La aprobación se basa en los datos de un ensayo en fase III que evalúa el medicamento cada cuatro semanas (200 mg o 300 mg en función del peso corporal) más corticoides tópicos (CET) de baja potencia versus CET solo (placebo) en 162 niños de seis meses a cinco años con dermatitis atópica de moderada a grave. A las 16 semanas, dupilumab mejoró el aclaramiento cutáneo y redujo la gravedad general de la enfermedad y el picor en comparación con el brazo placebo en el conjunto de la población.
En un subgrupo de pacientes con dermatitis atópica grave, el 46% de los pacientes aleatorizados a dupilumab alcanzó una mejora del 75% o superior en la gravedad general de la enfermedad en comparación con el 7% tratados con placebo; el 14% alcanzó una piel sin lesiones o casi sin lesiones; una reducción del 55% en la gravedad general de la enfermedad desde el inicio y una disminución media del picor del 42% con respecto al inicio en comparación con un aumento del 1% con placebo.
Aproximadamente siete veces más pacientes tratados con dupilumab -de entre seis meses y cinco años- experimentaron piel casi sin lesiones y una reducción de la gravedad general de la enfermedad
Dupilumab también mejoró la calidad del sueño, el dolor cutáneo y la calidad de vida relacionada con la salud en comparación con placebo, tanto en la población general como en la grave. Los datos de eficacia a largo plazo mostraron que el beneficio clínico a las 16 semanas se mantuvo durante 52 semanas.
Los efectos secundarios más frecuentes en todas las indicaciones incluyen reacciones en el lugar de la inyección, conjuntivitis, conjuntivitis alérgica, artralgia, herpes oral y eosinofilia. Los resultados de seguridad del ensayo de 6 meses a 5 años fueron generalmente coherentes con el perfil de seguridad conocido del medicamento en sus indicaciones aprobadas; en el ensayo, los acontecimientos adversos observados con más frecuencia con este tratamiento en comparación con placebo incluyeron eosinofilia y conjuntivitis. El perfil de seguridad a largo plazo hasta las 52 semanas fue similar al perfil de seguridad observado a las 16 semanas y coherente con lo observado en pacientes de mayor edad con dermatitis atópica.