Redacción
Químicos y biólogos del cáncer de Estados Unidos y Alemania han conseguido encontrar un camino que les permite afrontar el mayor desafío de investigación del cáncer, un oncogén llamado MYC, que impulsa el crecimiento desenfrenado de células cancerosas y que hasta ahora ha demostrado ser un objetivo farmacológico difícil, según publican en la revista Nature, en un trabajo que recoge Europa Press.
El gen del cáncer MYC ha sido bautizado como el “Monte Everest” de la investigación oncológica debido a la dificultad de diseñar medicamentos que puedan desactivarlo, y a la expectativa de que un fármaco eficaz contra MYC pudiera ayudar a tantos enfermos de cáncer. Ahora, la colaboración entre científicos especializados en ARN, químicos y biólogos del cáncer del Instituto Wertheim UF Scripps (Estados Unidos) y el Instituto Max Planck de Fisiología Molecular (Alemania) ha escalado esa cima, al tiempo que abre nuevas rutas para hacer cumbre en otras enfermedades igualmente difíciles de tratar.
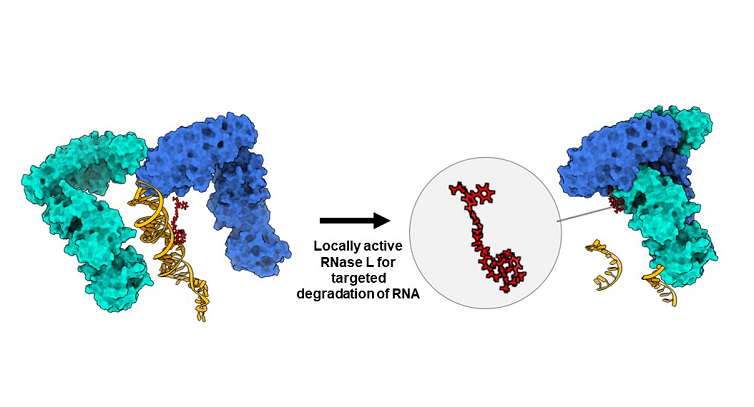
El nuevo enfoque dirige enzimas de reciclaje de las células hacia el ARN del oncogén MYC y corta segmentos clave para impedir que haga daño. Este método también ha funcionado con el oncogén JUN y el MIR155
El enfoque de los científicos dirige las enzimas de reciclaje de las células hacia el ARN de los genes cancerígenos y corta segmentos clave para impedir que hagan daño. La táctica funcionó contra el gen del cáncer MYC, y también contra otros dos genes del cáncer que suponen un reto, JUN y MIR155. Los tres genes del cáncer regulan la transcripción de otros genes, provocando un rápido crecimiento tumoral.
“Para los pacientes de cáncer cuya enfermedad está provocada por estos oncogenes tan comunes pero difíciles, el método del degradador de ARN puede ofrecer nuevas esperanzas“, afirma el doctor Herbert Waldmann, director del Instituto Max Planck de Fisiología Molecular de Dortmund (Alemania).
Su estudio también abre nuevas posibilidades para dirigir medicamentos contra el ARN, lo que potencialmente abre muchas otras enfermedades genéticas a este enfoque de tratamiento, destaca el químico y profesor Matthew D. Disney, del Instituto Herbert Wertheim UF Scripps de Innovación Biomédica y Tecnología y del Centro Oncológico de UF Health.
Dr. Waldmann: “Para los pacientes de cáncer cuya enfermedad está provocada por estos oncogenes tan comunes pero difíciles, el método del degradador de ARN puede ofrecer nuevas esperanzas”
“Descubrimos unas 2.000 nuevas estructuras de ARN capaces de unirse a pequeñas moléculas similares a fármacos e identificamos seis nuevos quimiotipos capaces de unirse al ARN”, explica. “Básicamente, hemos creado una enciclopedia de pliegues de ARN susceptibles de fármacos“.
Entre las dianas farmacológicas más difíciles, MYC es también una de las más importantes ya que su activación puede afectar al 70% o más de todos los cánceres humanos, puede dirigir la construcción o el silenciamiento de muchos otros genes, y afecta al crecimiento celular e incluso a un programa de suicidio celular que lleva a las células dañadas a autodestruirse, un proceso vital llamado apoptosis. También afecta al proceso de reparación del ADN dañado y al crecimiento de los vasos sanguíneos. En muchos cánceres MYC se sobreexpresa, lo que lleva a las células a crecer y dividirse con demasiada rapidez.
El oncogén MYC está entre las dianas farmacológicas más difíciles y su activación puede afectar al 70% o más de los cánceres
La activación de otro gen cancerígeno, JUN, se ha observado en más de 20 tipos distintos de cáncer, como glioblastoma, cáncer de mama, próstata, pulmón y colorrectal, entre otros. Por su parte, un pequeño gen ARN llamado MIR155 impulsa la inflamación y el crecimiento y la propagación de muchos tipos de cáncer. Los investigadores lo han encontrado activado en cánceres de mama, riñón, gástrico y otros.
Los esfuerzos por fabricar fármacos que impidan que los tres oncogenes causen daños han fracasado en gran medida, debido a sus complejos retos estructurales. El doctor Frank Glorius, químico orgánico del Instituto de Química Orgánica de la Universidad de Münster (Alemania), ha desarrollado métodos innovadores para construir nuevas moléculas similares a fármacos.
Los esfuerzos por fabricar fármacos que impidan que los tres oncogenes causen daños han fracasado en gran medida, debido a sus complejos retos estructurales
La idea de la asociación surgió por primera vez en 2016 durante una conferencia científica en España, cuando Waldmann y Disney compararon notas tras una charla. Ambos coincidieron en que dirigir fármacos contra el ARN podía ser una forma interesante de tratar enfermedades incurables, pero aún era pronto. No existía nada parecido en el mercado.
El ARN representaba un difícil reto farmacológico pero a lo largo de 15 años, Disney y su grupo han identificado muchas estructuras de ARN conservadas y susceptibles de fármacos y creado sus propias colecciones de compuestos y demostró en ratones que dirigirse a los ARN puede acabar con tumores cancerosos y mejorar otras enfermedades, como la ELA y la distrofia miotónica. El ARN ofrecía una vía alternativa para abordar enfermedades cuyas estructuras proteicas clave no podían ser alcanzadas por los medicamentos.
Un encuentro científico en España unión a los investigadores de Estados Unidos y de Alemania y juntos han creado colecciones de compuestos dirigidas a estructuras de ARN susceptibles a fármacos
Tras esa conversación inicial, en 2018 Disney envió a dos miembros de su laboratorio, los entonces estudiantes de posgrado Matthew Costales, y Hafeez Hanif, a Dortmund para utilizar sus métodos de cribado para cazar posibles candidatos de unión al ARN. Disney asegura que los resultados superaron sus expectativas. En total, sondearon más de 61 millones de interacciones entre las colecciones de compuestos y el ARN humano.
Cuando analizaron los resultados, descubrieron que el universo de estructuras de ARN conocidas y susceptibles de fármacos se había ampliado drásticamente. Pero harían falta varios años más de trabajo para conectar esas estructuras y los compuestos que encontraron con los difíciles objetivos oncológicos MYC, c-JUN y MIR155.
La doctora Jessica Childs-Disney y el estudiante Yuquan Tong, del laboratorio de Disney en el Instituto Wertheim UF Scripps, realizaron muchos de esos experimentos cruciales. “Descubrimos que no bastaba con unir el ARN de estas dianas. Eso por sí solo no tenía suficiente efecto. También tuvimos que modificar los compuestos para que pudieran reclutar enzimas de degradación de ARN de moléculas pequeñas”, explica Tong.
Han desarrollado una molécula híbrica denominada RiboTAC, con la que han eliminado tuomores de mama y linfomas de células B impulsados por MYC en ratones
Disney había ideado un método innovador para eliminar estos segmentos de ARN patógenos. Para ello, unió a las moléculas un anzuelo químico diseñado para atrapar las enzimas de reciclaje de ARN de la célula. Funcionó según lo previsto. La enzima de reciclaje del ARN troceó el ARN al que estaba unida la molécula del fármaco, impidiendo que se formaran las proteínas causantes de la enfermedad. Llamaron a su molécula híbrida RiboTAC, abreviatura de “quimera dirigida a ribonucleasas”.
“Con el degradador añadido, empezamos a ver cómo estos ARN cancerígenos ‘no tratables’ se reducían en un 35%, 40%, 50% o más. Esto provocó la muerte de las células cancerosas y eliminó los tumores en estudios con ratones sobre el cáncer de mama que se extendía a los pulmones”, explica Disney.
Dr. Cleveland: “se pueden diseñar degradadores de ARN específicos para desactivar muchos ARN oncogénicos, representan un paso verdaderamente transformador en la terapéutica anticancerosa”
Disney se puso en contacto con uno de los principales expertos en la función de MYC en el cáncer, el doctor John Cleveland, vicepresidente ejecutivo, director del centro y director científico de Moffitt Cancer Center en Tampa. “Nuestro laboratorio probó la eficacia de los compuestos RiboTAC diseñados para destruir el ARN MYC y demostró que eliminan eficazmente los linfomas de células B impulsados por MYC, que son tumores muy agresivos y difíciles de tratar”, apunta Cleveland. “Estos resultados, que ahora se pueden diseñar degradadores de ARN específicos para desactivar muchos ARN oncogénicos, representan un paso verdaderamente transformador en la terapéutica anticancerosa“.
Según Waldmann, el estudio demuestra que las clases de compuestos inspiradas en productos naturales ofrecen una fuente nueva y rica para atacar dianas de ARN contra enfermedades en general. Los compuestos están mostrando a los científicos hacia dónde dirigirse para fabricar más y mejores fármacos que combatan estas dianas del cáncer, antes imposibles, y proporcionando un banquete de nuevas estructuras de ARN que probar en otros escenarios de enfermedad.