Redacción
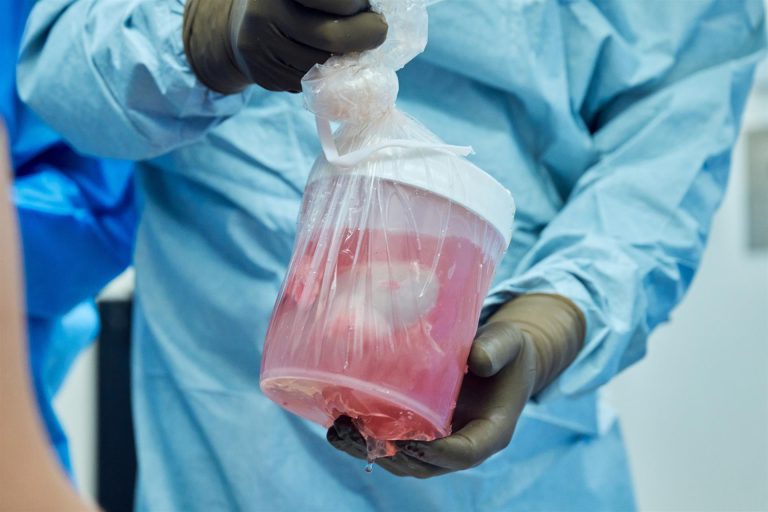
Un equipo de cirujanos del NYU Langone Health (Estados Unidos) ha trasplantado un riñón de cerdo modificado genéticamente que continúa funcionando bien después de 32 días en un hombre en muerte cerebral. Esto representa el período más largo en que un riñón de cerdo modificado genéticamente ha funcionado en un ser humano.
Cirujanos del NYU Langone Health han trasplantado un riñón de cerdo modificado genéticamente a un hombre en muerte cerebral
Los órganos procedían de animales que se habían modificado genéticamente para prevenir el rechazo por parte del sistema inmune del paciente, que tenía enfermedad renal. El paciente de 57 años fue declarado muerto por criterios neurológicos y se mantiene con un corazón latiente con asistencia respiratoria. Los investigadores en un artículo publicado en JAMA Surgery, los riñones trasplantados eran funcionales (podían fabricar orina y depurar creatinina) siete días después de la operación. El estudio continuará hasta mediados de septiembre de 2023.

“El trabajo demuestra que un riñón de cerdo, con solo una modificación genética y sin medicamentos ni dispositivos experimentales, puede reemplazar la función de un riñón humano durante al menos 32 días sin ser rechazado”, señala el Dr. Robert Montgomery, que ha dirigió el procedimiento. Además, anteriormente había realizado el primer trasplante de riñón de cerdo genéticamente modificado a un difunto humano el 25 de septiembre de 2021, seguido de un segundo procedimiento similar el 22 de noviembre de 2021. Los cirujanos del Transplant Institute realizaron dos trasplantes de corazón de cerdo genéticamente modificado en el verano de 2022.
Dr. Montgomery: “El trabajo demuestra que un riñón de cerdo, con solo una modificación genética y sin medicamentos ni dispositivos experimentales, puede reemplazar la función de un riñón humano durante al menos 32 días sin ser rechazado”
Eliminar un gen problemático se muestra prometedor
El primer obstáculo que hay que superar en los xenotrasplantes (trasplantes de órganos de animales a personas) es evitar el rechazo hiperagudo, que suele producirse pocos minutos después de que un órgano animal se conecte al sistema circulatorio humano. En los cinco xenotrasplantes realizados en el NYU Langone se ha evitado el rechazo inmediato eliminando el gen que codifica la biomolécula alfa-gal, responsable del rápido rechazo de los órganos porcinos mediado por anticuerpos. Además, la glándula timo del cerdo, responsable de educar el sistema inmunitario, se incrustó bajo la capa externa del riñón para evitar nuevas respuestas inmunitarias retrasadas. Se ha demostrado que esta combinación de modificaciones evita el rechazo del órgano al tiempo que preserva la función renal.
Para garantizar que la función renal del organismo se mantuviera únicamente con el riñón de cerdo, se extirparon quirúrgicamente los dos riñones nativos del receptor del trasplante. Después, se trasplantó un riñón de cerdo, que empezó a producir orina inmediatamente sin ningún signo de rechazo hiperagudo. Durante la fase de observación, el personal clínico de cuidados intensivos mantuvo al fallecido en soporte mientras se controlaba el funcionamiento del riñón de cerdo y se tomaban muestras con biopsias semanales. Los niveles de creatinina se mantuvieron dentro de los valores óptimos durante todo el estudio, y la biopsia no mostró indicios de rechazo.
En los cinco xenotrasplantes realizados en el NYU Langone se ha evitado el rechazo inmediato eliminando el gen que codifica la biomolécula alfa-gal
El riñón y la glándula timo utilizados en este procedimiento se obtuvieron de un cerdo GalSafe, un animal diseñado por la compañía Revivicor. En diciembre de 2020, la Administración de Drogas y Alimentos de Estados Unidos (FDA) aprobó el cerdo GalSafe como fuente potencial para terapias humanas, así como una fuente de alimento para las personas con síndrome alfa-gal, una alergia a la carne causada por una picadura de garrapata.
En anteriores trasplantes de órganos de cerdo modificados genéticamente se habían incorporado hasta 10 modificaciones genéticas. Sin embargo, este estudio demuestra que un riñón porcino de un solo gen modificado puede seguir funcionando óptimamente durante al menos 32 días sin rechazo.
El equipo de médicos utilizó medicamentos inmunosupresores estándar para el trasplante combinados con un mayor cribado del citomegalovirus porcino (pCMV) en el cerdo donante para garantizar la seguridad. Estudios recientes han demostrado que el pCMV puede afectar al rendimiento del órgano y desencadenar un posible fallo. No se detectó pCMV después de 32 días, y se llevó a cabo una estrecha vigilancia del retrovirus endógeno porcino (PERV), junto con otros seis virus de interés.