J.P.R.
El Sistema Nacional de Salud financiará teclistamab (Tecvayli) en monoterapia para el tratamiento de mieloma múltiple en recaída y refractario a partir de este 1 de mayo. Este anticuerpo biespecífico está dirigido a pacientes triple expuesto a tres clases terapéuticas: un agente inmunomodulador, un inhibidor del proteosoma y un anticuerpo anti-CD38.
La comercialización de este medicamento viene a abordar “una necesidad médica no cubierta”, ha explicado la Dra. María Victoria Mateos, responsable de la Unidad de Mieloma y Unidad de Ensayos Clínicos del Hospital Universitario de Salamanca, y presidenta de la Sociedad Española de Hematología y Hemotarapia (SEHH), durante una rueda de prensa organizada por Johnson & Johnson, compañía que ha desarrollado este medicamento.
Una revisión puso de manifiesto la heterogeneidad de tratamiento una vez que los pacientes habían agotado estas tres clases terapéuticas. “Nos encontramos con 100 regímenes diferentes. No había un estándar de tratamiento homogéneo con los pacientes que habían recibido estos tres tipos de fármacos”, expuso la Dra. Mateos.
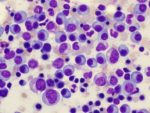
Teclistamab es un anticuerpo biespecífico redirige a los linfocitos T CD3 positivo hacia las células de mieloma que expresan BCMA para inducir la muerte de las células tumorales
El estudio evidenciaba que solo uno de cada tres pacientes tenían algún tipo de respuesta y la supervivencia libre de progresión (SLP) no superaba los cuatro meses. En concreto, esta terapia redirige a los linfocitos T CD3 positivo hacia las células de mieloma que expresan el antígeno de maduración de linfocitos B (BCMA) para inducir la muerte de las células tumorales.
“No disponíamos de opciones de tratamiento de rescate cuando los pacientes habían recibido estas tres clases de fármacos, que son los convencionales que utilizamos para el tratamiento del mieloma múltiple de nuevo diagnóstico y las primeras recaídas. Por lo tanto, las únicas posibilidades hasta ahora pasaban por reutilizar lo que se había utilizado previamente”, añadió la presidenta de la SEHH.
Los resultados del estudio MajesTEC-1 ponen de manifiesto que este anticuerpo biespecífico supone una nueva estrategia de rescate para pacientes y clínicos. El fármaco ha mostrado una tasa global de respuesta del 63%, una tasa de remisiones completas o mejores del 45,5% y supervivencia libre de progresión “muy positiva”. “Hemos tratado a pacientes en fases avanzadas de la enfermedad. Necesitábamos tratamientos que lograran respuestas rápidas. Teclistamab logra respuesta en un mes y en cuatro o cinco meses se consigue la remisión completa”, subrayó.
Dra. Mateos: “No disponíamos de opciones de tratamiento de rescate cuando los pacientes habían recibido estas tres clases de fármacos”
Los datos de MajesTEC-1 habrían sido más positivos de no ser por el Covid-19. El inicio de la segunda fase coincidió con la explosión de la pandemia en los países occidentales en marzo de 2020. En un análisis post hoc recientemente presentado, con el objetivo de evaluar este impacto en los resultados, se demostró que las medianas de duración de la respuesta (26.7 meses [21.6–NE]), supervivencia libre de progresión (15.1 meses [9.9–22.8]) y global (28.3 meses [21.9–NE]) se prolongaron cuando se censuraron por muertes por Covid-19.
Desde el comienzo de este ensayo clínico se han tratado más de 10.000 pacientes en todo el mundo con mieloma múltiple desde que el ensayo clínico coemnzara en 2016. España ha jugado un papel importante en el ensayo clínico. En concreto han participado 60 pacientes de siete centros hospitalarios diferentes. A estos se añaden otros 40 pacientes incluidos en el programa de acceso precoz.