..Cristina Cebrián.
Ya se encuentra disponible el fármaco alectinib, comercializado por Roche bajo el nombre de Alecensa y financiado por el Ministerio de Sanidad, Servicios Sociales e Igualdad. Se trata del primer inhibidor de la tirosina quinasa ALK con un mecanismo de acción selectivo que es capaz de entrar en el sistema nervioso central y ser activo frente a la metástasis cerebral en pacientes con cáncer de pulmón no microcítico (CPNM) ALK+.
Alectinib es el primer inhibidor de la tirosina quinasa ALK capaz de entrar en el sistema nervioso central y ser activo frente a la metástasis cerebral en pacientes con cáncer de pulmón no microcítico
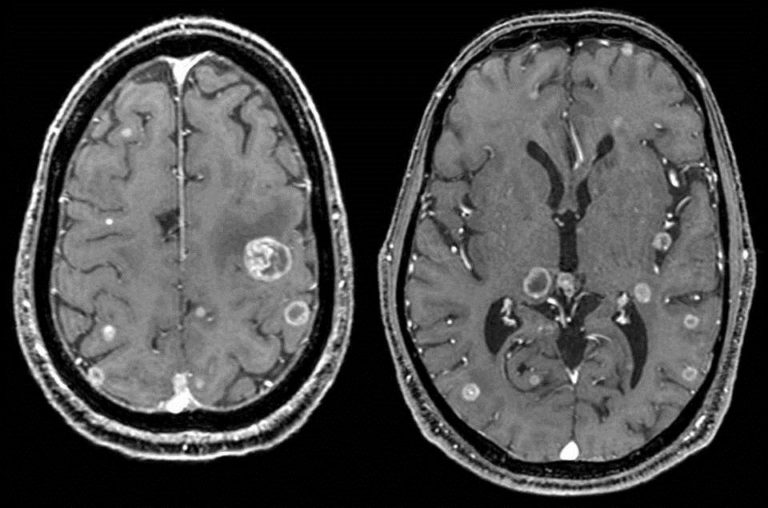
Cada año se diagnostican en el mundo unos 75.000 casos nuevos de este tipo de tumor y de éstos, 500 se producen en nuestro país. Se trata, por tanto, de un tipo de tumor poco frecuente y que suele afectar a mujeres con una media de 50 años y que son poco o nada fumadoras. La metástasis en el cerebro se produce en un 60% de los casos y se trata de una complicación difícil de tratar ya que las terapias disponibles no han sido capaces de traspasar la barrera hematoencefálica para atacar a las células tumorales.
Las metástasis cerebrales tienen mal pronóstico, ya que indican la presencia de un cáncer diseminado y, dependiendo de si el tumor primario está controlado o no, y del número de metástasis intracraneales (única o múltiples) se aplica un tratamiento u otro (radioterapia o cirugía).
La metástasis en el cerebro se produce en un 60% de los casos y se trata de una complicación difícil de tratar ya que las terapias disponibles no han sido capaces de traspasar la barrera hematoencefálica para atacar a las células tumorales
 Ahora, esta nueva terapia que se administra por vía oral consigue penetrar en el sistema nervioso central y ser activa contra las metástasis cerebrales. Por tanto, se reduce el riesgo de progresión cuando la patología aún no ha afectado al cerebro. Además, con este tratamiento se reducen los efectos secundarios. El Ministerio de Sanidad ha financiado el fármaco para las dos indicaciones que aprobó en 2017 la Agencia Europea del Medicamento (EMA). La primera de ellas, como tratamiento de primera línea en monoterapia para cáncer de pulmón no microcítico avanzado ALK+. Como terapia de segunda línea, la EMA lo aprobó en monoterapia para cáncer de pulmón no microcítico avanzado ALK+ en pacientes que han sido tratados previamente con crizotinib.
Ahora, esta nueva terapia que se administra por vía oral consigue penetrar en el sistema nervioso central y ser activa contra las metástasis cerebrales. Por tanto, se reduce el riesgo de progresión cuando la patología aún no ha afectado al cerebro. Además, con este tratamiento se reducen los efectos secundarios. El Ministerio de Sanidad ha financiado el fármaco para las dos indicaciones que aprobó en 2017 la Agencia Europea del Medicamento (EMA). La primera de ellas, como tratamiento de primera línea en monoterapia para cáncer de pulmón no microcítico avanzado ALK+. Como terapia de segunda línea, la EMA lo aprobó en monoterapia para cáncer de pulmón no microcítico avanzado ALK+ en pacientes que han sido tratados previamente con crizotinib.
Estudio en fase III ‘Alex’
El estudio internacional fase III ‘Alex’ demostró en su momento que este tratamiento era capaz de reducir en más de la mitad el riesgo de progresión o muerte frente a la terapia estándar con crizotinib. Además, el estudio concluyó que la tasa acumulada de progresión en el sistema nervioso central al año para pacientes con o sin metástasis iniciales fue del 9,45% en comparación con el 41,4% del tratamiento estándar.
El estudio concluyó que la tasa acumulada de progresión en el sistema nervioso central al año para pacientes con o sin metástasis iniciales fue del 9,45% en comparación con el 41,4% del tratamiento estándar
El doctor Javier de Castro, jefe de sección de Oncología Médica del Hospital La Paz de Madrid señaló que este efecto preventivo del fármaco sobre las metástasis cerebrales puede significar “un cambio en la historia natural de la enfermedad”, ya que esta afectación “empeora la calidad de vida y la supervivencia de los pacientes de forma significativa”.
Por su parte, el jefe del Servicio de Oncología del Hospital 12 de Octubre de Madrid, Luis Paz Ares, declaró que los datos del estudio ponen de manifiesto la superioridad de este nuevo fármaco, tanto en primera como en segunda línea, por lo que ahora lo realmente importante es la secuencia en que se administran las diferentes alternativas que hay disponibles.