..Redacción.
Diez hospitales españoles llevarán a cabo el primer ensayo clínico aprobado en España sobre la eficacia de anakinra en el tratamiento del Covid-19. Tras la autorización de la Agencia Española de Medicamentos y Productos Sanitarios (Aemps), el Grupo de Enfermedades Autoinmunes Sistémicas (GEAS) de la Sociedad Española de Medicina Interna (SEMI) pone en marcha la investigación.
Anakinra, comercializado como Kineret, es un fármaco indicado para las enfermedades autoinflamatorias y ahora podría reducir la respuesta inflamatoria exagerada y la neumonía en pacientes graves por Covid-19 con el “síndrome de tormenta de citoquinas”.
El objetivo es evaluar el efecto de anakinra añadido al tratamiento estándar, en la necesidad de ventilación mecánica en pacientes con neumonía grave por Covid-19
El ensayo clínico está financiado por la biofarmacéutica Sobi y tiene dos objetivos principales. Por un lado, evaluar el efecto de anakinra añadido al tratamiento estándar, en la necesidad de ventilación mecánica en pacientes con neumonía grave por Covid-19 y tormenta de citoquinas;. Por otro lado, pretende analizar el efecto del fármaco sobre la mortalidad en estos pacientes con Covid-19 y tormenta de citoquinas.
Los diez hospitales que participan en el estudio han recopilado datos que sostienen que alrededor del 20% del total de sus pacientes con Covid-19 desarrollan esta “tormenta de citoquinas”. Además, las observaciones clínicas actuales apuntan a que, tras una primera fase vírica causada por la infección por SARS-CoV-2, en un subgrupo de pacientes se activa el sistema inmune generando una respuesta inmunitaria excesiva y descontrolada.
 Dra. Fanlo: “La IL-1 tiene una importante relevancia patogénica dado que promueve la cascada inflamatoria e induce asimismo la síntesis de varios genes inflamatorios como la IL-6”
Dra. Fanlo: “La IL-1 tiene una importante relevancia patogénica dado que promueve la cascada inflamatoria e induce asimismo la síntesis de varios genes inflamatorios como la IL-6”
Esta respuesta se asocia con una hiperinflamación y la aparición del síndrome de insuficiencia respiratoria aguda o Síndrome de Distrés Respiratorio del Adulto (SDRA). Este se ha descrito como la principal causa de mortalidad por Covid-19. En España, el SDRA lo ha padecido el 4,8% de entre los primeros 18.609 casos con información completa de los que se dispone.
Reducir la tormenta de citoquinas
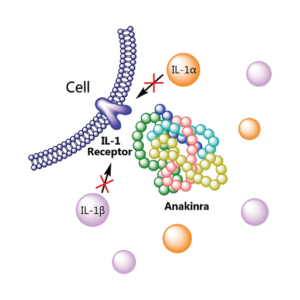
La coordinadora del GEAS y de la Unidad de Enfermedades Autoinmunes Sistémicas del Complejo Hospitalario de Navarra y líder de este estudio, la Dra. Patricia Fanlo, explica que un subgrupo de pacientes con Covid-19 muestra una elevación muy marcada de parámetros inflamatorios. Además, en ese grupo existe una importante liberación de citoquinas proinflamatorias, incluidas la interleuquina (IL-1) y la interleuquina (IL-6).
“La IL-1 tiene una importante relevancia patogénica dado que promueve la cascada inflamatoria e induce asimismo la síntesis de varios genes inflamatorios como la IL-6. En este sentido, este antagonista recombinante del receptor de la IL-1 podría reducir la tormenta de citoquinas desencadenada. También podría prevenir la necesidad de ventilación mecánica en los pacientes graves”, detalla la especialista.
Dr. Vila: “Una de las hipótesis sobre el Covid-19 es que la IL-1 es una de las citoquinas clave en la respuesta inflamatoria excesiva y descontrolada”
Por su parte, el director médico de Sobi en España y Portugal, el Dr. Juan Vila, señala que “una de las hipótesis sobre la enfermedad es que la IL-1 es una de las citoquinas clave en la respuesta inflamatoria excesiva y descontrolada que están sufriendo algunos de los pacientes que han desarrollado neumonía por Covid-19. Por ello, desde GEAS y Sobi se ha considerado que podría tener un papel beneficioso en el tratamiento de la infección por Covid-19”.
Fases del ensayo clínico con anakinra
El ensayo clínico constará de tres fases. La primera consistirá en un periodo de selección, una segunda de tratamiento de dos semanas y la tercera de seguimiento de dos semanas más.
 El periodo de tratamiento de dos semanas es abierto y los pacientes serán asignados al azar al tratamiento con este antagonista del receptor de la IL-1 añadido al tratamiento estándar o tratamiento estándar solo en una proporción de 1:1. Se administrará en infusiones intravenosas cuatro veces al día (100mg/6 horas) durante un máximo de 15 días, según el estado de salud del paciente y la opinión clínica de los expertos. El criterio de valoración primario se evaluará en el día 15 y el 28.
El periodo de tratamiento de dos semanas es abierto y los pacientes serán asignados al azar al tratamiento con este antagonista del receptor de la IL-1 añadido al tratamiento estándar o tratamiento estándar solo en una proporción de 1:1. Se administrará en infusiones intravenosas cuatro veces al día (100mg/6 horas) durante un máximo de 15 días, según el estado de salud del paciente y la opinión clínica de los expertos. El criterio de valoración primario se evaluará en el día 15 y el 28.
Si se demuestra la utilidad del medicamento en esta enfermedad, los médicos podrían solicitar su empleo como uso compasivo cuando fuese necesario
Desde GEAS y Sobi esperan tener disponibles los resultados en unos meses, aunque se cuenta con obtener un análisis preliminar en apenas unas semanas. Si se demuestra la utilidad del medicamento en esta enfermedad, los médicos podrían solicitar su empleo como uso compasivo cuando fuese necesario, dado que es un medicamento que está comercializado en España desde 2002.
Por último, los diez hospitales españoles que participan en la investigación son: el Hospital Clínico Universitario de Santiago; Son Espases de Mallorca, el Complejo Hospitalario de Navarra: el Hospital La Fe de Valencia; el Vall d’Hebron y el Clínic de Barcelona; el Hospital La Paz de Madrid; el Clínico Universitario Lorenzo Blesa de Zaragoza; el Ramón y Cajal de Madrid y el Hospital Álvaro Cunqueiro de Vigo.