..Gema Maldonado.
Puede ser una de las noticias del año en el ámbito de la medicina de precisión. Son los primeros resultados del estudio de fase I que aplica por primera vez técnicas de edición genética CRISPR-Cas9 in vivo en pacientes con amiloidosis hereditaria por transtiretina (AhTTR), una enfermedad rara grave, para reducir la concentración de TTR en suero.
Se han publicado resultados preliminares de un fármaco basado en CRISPR-Cas9 mediante infusión en sangre para reducir los niveles séricos de proteína TTR en pacientes con amiloidosis hereditaria
Esta proteína, que principalmente se sintetiza en el hígado, cuando presenta una alteración genética se agregan en fibrillas que se deposita en diferentes sistemas y órganos. Principalmente, en el corazón y en el sistema nervioso periférico y central. Esta enfermedad tiene carácter progresivo y desemboca en la muerte entre dos y seis años después de su diagnóstico en pacientes con miocardiopatía amiloide y entre cuatro y 17 años en pacientes con polineuropatía amiloide sin miocardiopatía.
Los investigadores del ensayo, publicado el pasado sábado en The New England Journal of Medicine (NEJM), han infundido el fármaco de edición de genes in vivo NTLA-2001 por vía intravenosa a seis pacientes con esta enfermedad. A los 28 días de la inyección, la concentración de proteína TTR en los pacientes que recibieron una dosis de 0,1 mg por kilogramo presentaba una reducción del 52% y en quienes recibieron 0,3 mg por kilogramos alcanzó el 87%. Uno de los pacientes llegó a tener una reducción en sus niveles séricos de proteína TTR del 96%. Además, durante esas cuatro semanas, los eventos adversos en los seis pacientes fueron pocos y leves.
A los 28 días de la inyección se consiguieron reducciones de proteínas TTR del 52% y del 87% con una dosis de 0,1 mg/kg y 0,3 mg/kg, respectivamente
Los estudios preclínicos ya habían tenido resultados positivos y duraderos. Tanto en modelos de ratón transgénicos como en primates no humanos, concretamente monos cynomolgus, con una única dosis, obtuvieron reducciones de la proteína TTR del 95%. Es un porcentaje mayor al que proporcionan las terapias disponibles actualmente.
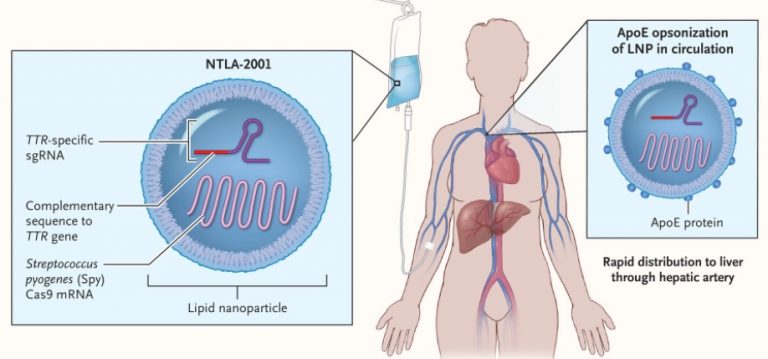
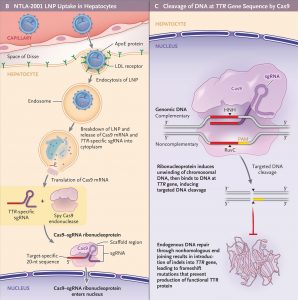
Los autores del ensayo explican cómo funciona el fármaco NTLA-2001. Se trata de un sistema de liberación de nanopartículas lipídicas dirigidas al hígado. Llevan un ARN guía único que se dirige a inactivar la proteína TTR y una secuencia de ARNm optimizada para la proteína Cas9. Esta terapia logra una disminución en la producción de TTR después de una sola administración. La amiloidosis hereditaria TTR es una candidata ideal para aplicar esta terapia de edición de genes in vivo, ya que se trata de una enfermedad monogénica.
La amiloidosis hereditaria TTR es una candidata ideal para aplicar esta terapia basada en CRISPR-Cas9, ya que se trata de una enfermedad monogénica
Los datos provisionales del estudio se presentaron el sábado en el encuentro anual de la Peripheral Nerve Society (PNS). El estudio está financiado por las desarrolladoras de la terapia, las compañías Intellia Therapeutics y Regeneron Pharmaceuticals. El presidente de Intellia, John Leonard, ha destacado que tras lograr una terapia dirigida al hígado basada en edición de genes mediante CRISPR-Cas9, se “abre la puerta al tratamiento de una amplia gama de otras enfermedades genéticas con nuestra plataforma modular”. De hecho, esperan “avanzar y expandir” su cartera de terapias “rápidamente”. “Con estos datos, creemos que realmente estamos abriendo una nueva era de la medicina”, aseveró.
El ensayo continúa con un aumento de dosis del fármaco para determinar si se podrían obtener mejores resultados en la reducción de proteínas TTR. Los investigadores están reclutando una tercera cohorte de pacientes para evaluar NTLA-2001 en dosis de 1mg por kilogramo.
Noticias complementarias:
- Dr. Manuel Romero: “La amiloidosis hereditaria por transtiretina, una enfermedad con un retraso diagnóstico de cuatro o cinco años”
- Amiloidosis hereditaria por transtiretina, una enfermedad no tan rara en dos puntos de España
- Los avances genéticos y las técnicas de imagen revolucionan el diagnóstico de la amiloidosis cardiaca
- La CUN participa en un ensayo clínico para tratar la amiloidosis, enfermedad rara que deteriora los órganos vitales