..G.M.
Aún no tiene cura y es uno de los grandes desafíos de la ciencia biomédica: el cáncer de mama metastásico. Pero cada nuevo encuentro internacional de profesionales especializados en este tipo de tumores avanzados culmina con resultados esperanzadores de nuevos tratamientos que pueden mejorar la supervivencia de las pacientes y su calidad de vida. Y esa es la esperanza que ha generado el fármaco trastuzumab deruxtecan (T-Dxd) en los médicos que han participado, y siguen participando. en los ensayos clínicos en pacientes con cáncer de mama no resecable o metastásico HER2 positivo, que previamente habían sido tratados con trastuzumab y un taxano.
El estudio Destinity Breast03 que evalúa el tratamiento con T-DXd demostró una mayor tasa de supervivencia libre de progresión y de respuesta objetiva
Los resultados del estudio Destinity Breast03, un estudio randomizado de fase 3 que evalúa el tratamiento con T-DXd ofrecen “una impresionante mejora sin precedentes”, en opinión del Dr. Javier Cortés, director del Centro Internacional del Cáncer de Mama del Hospital Universitario Vall d’Hebron (Barcelona). El tratamiento demostró una mayor tasa de supervivencia libre de progresión y de respuesta objetiva en los subgrupos de pacientes tratadas con T-DXd en comparación con trastuzumab emtansina (T-DM1).
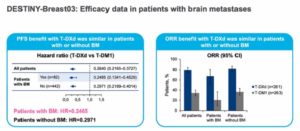
El 75,8% de las pacientes a las que se les administró T-DXd alcanzaron 12 meses de supervivencia libre de progresión de la enfermedad en comparación con el 34,1% que alcanzó este objetivo de entre las tratadas con T-DM1.
El 75,8% de las pacientes a las que se les administró T-DXd alcanzaron 12 meses de supervivencia libre de progresión. Especialmente significativa fue la respuesta en las pacientes con cáncer de mama con metástasis cerebrales
Especialmente significativa fue la respuesta en las pacientes con metástasis cerebrales. “T-DXd resultó en un gran control de la enfermedad comparado con T-DM1. Además se asoció a una sustancial respuesta intracraneal y a una reducción de la enfermedad en el sistema nervioso central”, explicó el Dr. Cortés.
La respuesta intracraneal para T-DXd fue del 27,8% frente al 2,8% para T-DM1. En paciente sin metástasis cerebrales también consiguió controlar la enfermedad. El medicamento, además, “demostró una tolerabilidad y perfil de seguridad comparable a T-DM1”. El oncólogo del Vall d´Hebron concluyó que estos datos “apoyan la idea de que T-DXd se convierta en el tratamiento habitual de segunda línea en cáncer HER2 positivo con metástasis cerebral”.
Dr. Cortés: “Estos datos apoyan la idea de que T-DXd se convierta en el tratamiento habitual de segunda línea en cáncer de mama HER2 positivo con metástasis cerebral”
 Este anticuerpo conjugado se utiliza desde 2020 en vida real en Francia por la vía de autorización de uso temporal. Esto ha permitido realizar un estudio sobre T-DXd en vida real, cuyos primeros datos presentó este lunes la Dra. Veronique Dieras, oncóloga del Centro Eugène-Marquis de Rennes, en Francia. “En seis meses se enrolaron 468 pacientes y más de 300 médicos de 155 pacientes solicitaron el medicamento para sus pacientes”, ha contado la doctora.
Este anticuerpo conjugado se utiliza desde 2020 en vida real en Francia por la vía de autorización de uso temporal. Esto ha permitido realizar un estudio sobre T-DXd en vida real, cuyos primeros datos presentó este lunes la Dra. Veronique Dieras, oncóloga del Centro Eugène-Marquis de Rennes, en Francia. “En seis meses se enrolaron 468 pacientes y más de 300 médicos de 155 pacientes solicitaron el medicamento para sus pacientes”, ha contado la doctora.
Estos datos “ilustran la necesidad médica no cubierta en esta población que ya ha sido tratada. Muchos de estos pacientes recibieron previamente trastuzumab, pertuzumab y T-DM1”. Los resultados hasta ahora muestran una actividad antitumoral con una tasa de respuesta del 56,7%. “Pese a que el tiempo de media que llevan en tratamiento es de 1,9 meses, es poco, más de la mitad ha respondido a la medicación”, añadió la oncóloga. El perfil de seguridad de T-DXd fue “manejable y sin nuevos signos de seguridad observados”, concluyó.
Noticias complementarias:
- AstraZeneca y Daiichi Sankyo lanzan una campaña de concienciación sobre el cáncer de mama metastásico
- Trastuzumab deruxtecán reduce en un 72% el riesgo de progresión o muerte por cáncer de mama metastásico HER2 positivo
- Trastuzumab deruxtecan muestra resultados positivos en tres tumores con alteraciones en HER2
- Los nuevos fármacos inmunoconjugados y sus resultados en cáncer de mama HER2












