Redacción
Investigadores del Consejo Superior de Investigaciones Científicas (SCIC) han creado cápsulas capaces de liberar células CAR-T para tratar de forma más específica y efectiva tumores sólidos. Así, la terapia con células CAR-T constituye una nueva forma de abordar el tratamiento contra el cáncer. Además, ha demostrado su potencial en el ámbito de la oncohematología, pero no tanto en tumores sólidos.
La gran mayoría de los tumores diagnosticados son sólidos
La dificultad de las células CAR-T para viajar a través de los tejidos y llegar al tumor, así como la acción del ambiente hostil de los tumores ante ellas, suponen una barrera que frena el éxito de estas terapias avanzadas en tumores sólidos. Debido a que la gran mayoría de los tumores diagnosticados son de este tipo, desarrollar métodos que permitan incrementar la disponibilidad de células CAR-T en su interior para mejorar su eficacia es un objetivo prioritario a nivel clínico.
Como un “caballo de Troya” que permite esconder y proteger a sus “soldados” hasta el momento de la lucha, estas cápsulas cargadas de células CAR-T y un cóctel de biomoléculas que ayudarán a su acción eficaz, posibilitaran una liberación dirigida de los “soldados” en el tumor. De esta manera, les permite superar el ambiente hostil que los rodeará para llevar a cabo de forma eficiente su acción anti-tumoral.
El proyecto CARTsol está financiado por el Ministerio de Ciencia e Innovación con 994.000 de euros. En él participan el Centro de Investigación contra el Cáncer de Salamanca (CIC)), el Centro de Investigación Biomédica en Red de Cáncer (Ciberonc), la Universidad de Santiago de Compostela (USC) y el Centro de Investigaciones Médicas Avanzadas (CIMA) de Pamplona.
Las cápsulas están formadas por biopolímeros porosos y flexibles capaces de albergar un cóctel de biomoléculas
Incorporación de nanomateriales en biopolímeros
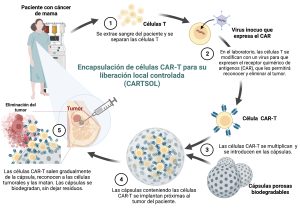 Las cápsulas están formadas por biopolímeros porosos y flexibles capaces de albergar un cóctel de biomoléculas. Estas cápsulas serán implantadas en las inmediaciones de una zona tumoral o en la región misma de la resección tras la extirpación quirúrgica del tumor. El objetivo es que las células CAR-T puedan liberarse lo más cerca posible de las células tumorales para reconocerlas específicamente y destruirlas.
Las cápsulas están formadas por biopolímeros porosos y flexibles capaces de albergar un cóctel de biomoléculas. Estas cápsulas serán implantadas en las inmediaciones de una zona tumoral o en la región misma de la resección tras la extirpación quirúrgica del tumor. El objetivo es que las células CAR-T puedan liberarse lo más cerca posible de las células tumorales para reconocerlas específicamente y destruirlas.
Las cápsulas podrán también incorporar nanopartículas magnéticas que permitan, tras una estimulación externa por el personal médico, destruir “quemando” las células tumorales residuales que queden tras la acción de las células CAR-T mediante la generación de altas temperaturas en la región donde están localizadas las cápsulas. Mediante técnicas de imagen el uso de estas cápsulas permitirá realizar un seguimiento en tiempo real de las células en el organismo. Por otra parte, los materiales que componen las cápsulas reducen posibles complicaciones como la aparición de fibrosis. Además, dada su flexibilidad, permitirán su implantación y extracción mediante técnicas de laparoscopia estándar en la práctica clínica.
El uso de estas cápsulas permitirá realizar un seguimiento en tiempo real de las células CAR-T en todo el organismo de los pacientes
Así, la clave del proyecto consiste en el diseño de la cápsula “similar a un caballo de Troya, que permite trasladar a salvo a los soldados al centro del campo de batalla y facilitarles armas abundantes, para que una vez fuera, maximicen su efecto contra las células tumorales“, explica José Rivas Rey, coordinador del proyecto. “Es una herramienta cuya arquitectura consiste en una cápsula porosa. Está elaborada por una mezcla de biopolímeros y es capaz de albergar un hidrogel enriquecido que permite incubar y expandir las células CAR-T, al tiempo que libera fármacos que debiliten al tumor”, añade.
En palabras de Xosé Bustelo, investigador principal del proyecto que trabaja en el Centro de Investigación del Cáncer de Salamanca y el Ciberonc, con esta metodología es posible “introducir e incubar células CAR-T plenamente activas en unas cápsulas que permitan su liberación efectiva y su acción anti-tumoral a largo plazo. Esto se realiza a través de la inclusión en las cápsulas de biomoléculas que facilitarán la liberación sin problemas de las células CAR-T y su proliferación dentro del tumor. Además, lo que es más importante, es que su acción anti-tumoral no sea bloqueada por las propias células tumorales. Usando un símil bélico, es como poder bombardear toda una zona de guerra tras haber inactivado las defensas antiaéreas del tumor”.
Los materiales que componen las cápsulas reducen posibles y su flexibilidad permitirá su implantación y extracción mediante técnicas de laparoscopia
“Como modelo de trabajo usaremos modelos de ratón de cáncer de mama. Estos serán tratados con células CAR-T modificadas genéticamente para que reconozcan moléculas que se expresan en estos tumores tumores”, indica Sandra Hervás, investigadora principal del proyecto. “Lo importante es que los métodos optimizados en este proyecto servirán para otros tipos de tumores sólidos“, añade.
Tras su optimización a nivel experimental, esta nueva versión de inmunoterapia será producida en modo GMP para su posible traslación al ámbito clínico. Esta tarea estará a cargo de la empresa pública gallega de servicios sanitarios Galaria, con su Unidad de producción de células CAR-T.
El proyecto Encapsulación de células CART en sistemas porosos nanoestructurados bioactivos para su liberación dirigida en tumores sólidos acaba de recibir financiación por parte de la Agencia Estatal de Investigación del Ministerio de Ciencia e Innovació, dentro del Programa Líneas Estratégicas 2022. Este programa está dotado con los Fondos de Reconstrucción y Resiliencia procedentes de la Unión Europea. La financiación global para el proyecto es de un millón de euros.














