Redacción
La técnica Crispr alcanzó la fama científica por su capacidad para editar genes con rapidez y precisión. Sin embargo, en el fondo, los sistemas Crispr son sistemas inmunitarios que ayudan a las bacterias a protegerse de los virus dirigiéndose y destruyendo el ADN y el ARN virales, según ha demostrado un nuevo estudio publicado en la revista ‘Science’. El nuevo trabajo revela la existencia de un actor hasta ahora desconocido en uno de estos sistemas, una proteína de membrana que mejora la defensa antivírica.
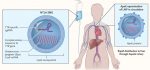
Los sistemas Crispr constan de dos componentes principales: un ARN guía que se dirige a una secuencia específica de ADN o ARN viral y una enzima Cas que corta el ADN o ARN objetivo, impidiendo que el virus se replique y propague. Un equipo del Centro de Biología del ARN de la Universidad de Rochester descubrió que una proteína Cas específica (Cas13b) no sólo corta el ARN vírico, sino que se comunica con otra proteína (Csx28) para aumentar su defensa antivírica.
El estudio del Centro de Biología del ARN de la Universidad de Rochester se ha publicado en la revista científica Science
En colaboración con científicos de Cornell, el equipo descubrió que la proteína Csx28 forma una estructura similar a un poro. Cuando infectaron ‘E. coli’ con un fago y desplegaron el sistema Crispr-Cas13 para atacar y detener la infección, descubrieron que Cas13 envía señales a Csx28 para afectar a la permeabilidad de la membrana. Una vez que esto sucede, Csx28 causa estragos en la célula infectada, desorganizando el potencial de membrana, aplastando el metabolismo y obstaculizando la producción de energía. Un virus no puede replicarse en circunstancias tan inhóspitas, lo que lleva al equipo a la conclusión de que Csx28 mejora la defensa contra fagos de Crispr-Cas13b.
“Este hallazgo contradice la idea de que los sistemas Crispr montan su defensa sólo degradando el ARN y el ADN en las células y realmente amplía nuestra visión de cómo los sistemas Crispr pueden estar funcionando”, destaca el autor correspondiente Mitchell O’Connell, miembro del Centro de la UR para la Biología del ARN. “Cuando pensamos en Crispr, vemos las proteínas Cas como Cas9 o Cas13 como el gran martillo que hace todo el daño, pero eso podría no ser el caso. Encontramos que Cas13 y Csx28 trabajan juntos para extinguir eficazmente un virus”, añade.
El equipo descubrió que cuando Cas13 no está presente, Csx28 no está activa
Con el conocimiento añadido de la estructura de Csx28 mediante el uso de crio-EM de alta resolución, el equipo está empezando a sondear la función de la proteína y surgieron numerosas preguntas como, si el objetivo es la protección, por qué hay un agujero gigante en la membrana.
El equipo descubrió que cuando Cas13 no está presente, Csx28 no está activa. ¿Qué hace que se active para defenderse? ¿Cuánto tiempo permanece activa y qué deja pasar a través de la membrana? Comprender la bioquímica que hay detrás de la apertura y cierre del poro arrojará luz sobre cómo Crispr-Cas13 lo utiliza como parte de su defensa y proporcionará un punto de partida para el estudio de las proteínas de membrana en otros sistemas Crispr.
“Este hallazgo es inesperado y plantea todo tipo de cuestiones nuevas sobre cómo se protegen las bacterias y qué hacen para sobrevivir a la infección”, señala Mark Dumont, profesor de Bioquímica y Biofísica del URMC que ha dedicado su carrera al estudio de las proteínas de membrana.