Redacción
Johnson & Johnson ha anunciado que el Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea de Medicamentos (EMA) ha recomendado la Autorización de Comercialización (MA) de Yuvanci, una terapia combinada en un solo comprimido que contiene macitentán 10 mg y tadalafilo 40 mg. Esta terapia está destinada al tratamiento a largo plazo de la Hipertensión Arterial Pulmonar (HAP) en pacientes adultos con Clase Funcional (CF) II o III según la clasificación de la Organización Mundial de la Salud (OMS), que ya estén recibiendo ambos medicamentos por separado.
Asimismo, la solicitud de autorización se basa en los datos del estudio A DUE de fase 3, un ensayo multinacional, multicéntrico, doble ciego, adaptativo, aleatorizado y controlado, que incluyó a 187 pacientes adultos con HAP (CF II-III de la OMS). Este estudio comparó la eficacia y seguridad de un comprimido único frente a las monoterapias de macitentán y tadalafilo. El estudio cumplió su criterio principal al demostrar una mejora significativa en la hemodinámica pulmonar, evidenciada por una reducción estadísticamente significativa y consistente de la resistencia vascular pulmonar (RVP) en comparación con las monoterapias a las 16 semanas.
El tratamiento con el comprimido único mostró una reducción del 29% en la RVP frente a macitentán y del 28% frente a tadalafilo
El tratamiento con el comprimido único mostró una reducción del 29% en la RVP frente a macitentán y del 28% frente a tadalafilo. Los resultados fueron consistentes en todos los subgrupos de edad, sexo, raza y Clase Funcional inicial de la OMS, así como en pacientes sin tratamiento previo y aquellos expuestos anteriormente a un antagonista del receptor de endotelina (ARE) o a un inhibidor de la fosfodiesterasa tipo 5 (PDE5i).
Los efectos adversos graves más frecuentes incluyeron anemia, palpitaciones, hipotensión, sangrado intermenstrual, edema/retención de líquidos y gripe. Además de Los efectos adversos más comunes observados fueron anemia/disminución de hemoglobina, edema/retención de líquidos y dolor de cabeza.
Los efectos adversos graves más frecuentes incluyeron anemia, palpitaciones, hipotensión, sangrado intermenstrual, edema/retención de líquidos y gripe
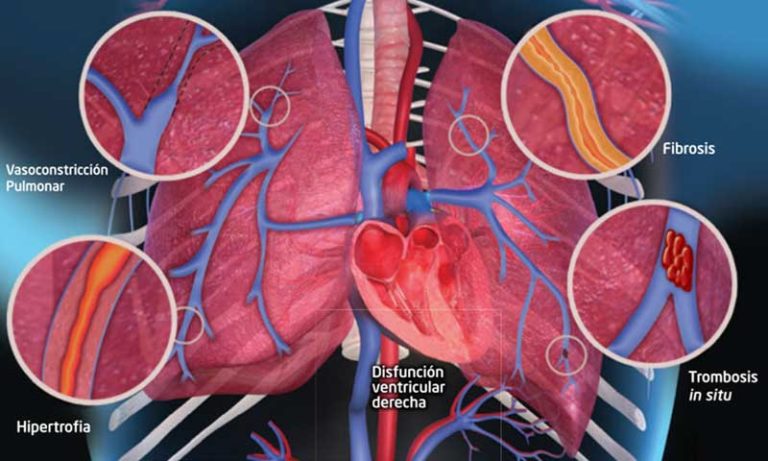
La HAP es una enfermedad rara, progresiva y potencialmente mortal, caracterizada por el estrechamiento de las pequeñas arterias pulmonares y la elevación de la presión sanguínea en la circulación pulmonar, lo que puede llevar a insuficiencia cardíaca derecha y muerte. Las guías de hipertensión pulmonar de la Sociedad Europea de Cardiología (ESC) y la Sociedad Respiratoria Europea (ERS) de 2022 ya recomendaban la combinación inicial de macitentán y tadalafilo para pacientes con HAP sin comorbilidades cardiopulmonares. Actualmente, estos pacientes deben tomar varios comprimidos, ya que no existe un tratamiento combinado en un solo comprimido en Europa.
Tamara Werner-Kiechle, M.D., responsable del área Cardiovascular y de Neurociencias de Johnson & Johnson Innovative Medicine en la región de EMEA, declaró: “La HAP es una enfermedad devastadora que afecta a personas de todas las edades. Introducir esta combinación sigue las pautas ESC/ERS y puede representar una nueva opción de tratamiento para los adultos que viven con HAP y que se enfrentan a regímenes de tratamiento complejos”.
“Esta opinión positiva representa un avance significativo y subraya nuestro compromiso de proporcionar soluciones para los pacientes con HAP”
Además, James F. List, M.D., Ph.D., jefe Global de Área Terapéutica de Investigación y Desarrollo de J&J Innovative Medicine, afirmó que “Esta opinión positiva representa un avance significativo y subraya nuestro compromiso de proporcionar soluciones para los pacientes con HAP. Esperamos colaborar con las autoridades sanitarias para hacer llegar nuestra terapia a los pacientes adultos que la necesitan en toda la región lo antes posible”.
A la espera de la aprobación de la Comisión Europea (CE), Yuvanci se convertiría en la única terapia combinada en un solo comprimido en Europa para el tratamiento de la HAP, cubriendo potencialmente todas las vías de tratamiento recomendadas por las guías. Esta opinión positiva del CHMP sigue a la aprobación de Opsynvi (macitentán y tadalafilo) por parte de la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) en marzo de 2024 para el tratamiento de pacientes con HAP.