..Redacción.
Investigadores de la Universidad de Stanford (Estados Unidos) han desarrollado un método de administración de las terapias CAR-T mediante un hidrogel que mejora el poder de ataque de las células T modificadas en tumores sólidos. Por el momento, los investigadores han obtenido resultados muy prometedores en ratones. La investigación se publicó el pasado viernes en la revista Science Advances.
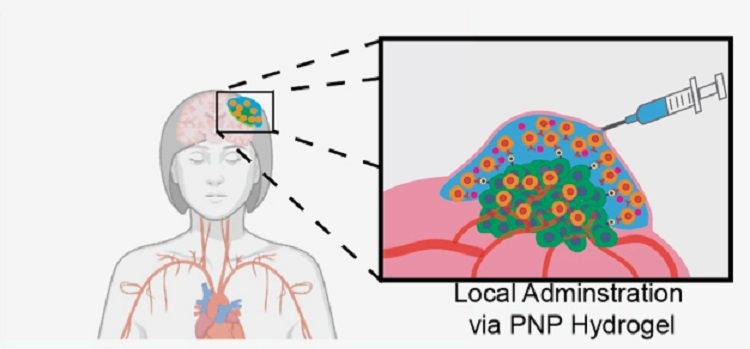
Las terapias CAR-T están ofreciendo buenos resultados en enfermedades oncológicas de la sangre y, aunque se está estudiando su utilización frente a tumores sólidos, aún no son una nueva alternativa terapéutica en estos cánceres. Los investigadores de Stanford han desarrollado un hidrogel basado en agua y con características en común con los tejidos biológicos. En este gel han agregado las células CAR-T y proteínas de señalización, las citoquinas, y lo han inyectado junto al tumor en ratones.
Han desarrollado un hidrogel al que agregan las células CAR-T y proteínas de señalización, las citoquinas, y lo han inyectado junto a tumores sólidos en ratones
Según explica la Universidad de Stanford, este gel proporciona un entorno temporal dentro del cuerpo del paciente en el que las células inmunitarias se multiplican y se activan para combatir las células cancerosas. Llegado el momento, las CAR-T son capaces de “romper” la barrera del hidrogel para ir atacando al tumor. “Gran parte del campo de las células CAR-T se centra en cómo hacer mejores células, pero hay mucho menos enfoque en cómo hacer que las células sean más efectivas una vez en el cuerpo”, afirma Eric Appel, autor principal del artículo. “Lo que estamos haciendo es totalmente complementario a todos los esfuerzos para diseñar mejores células”.
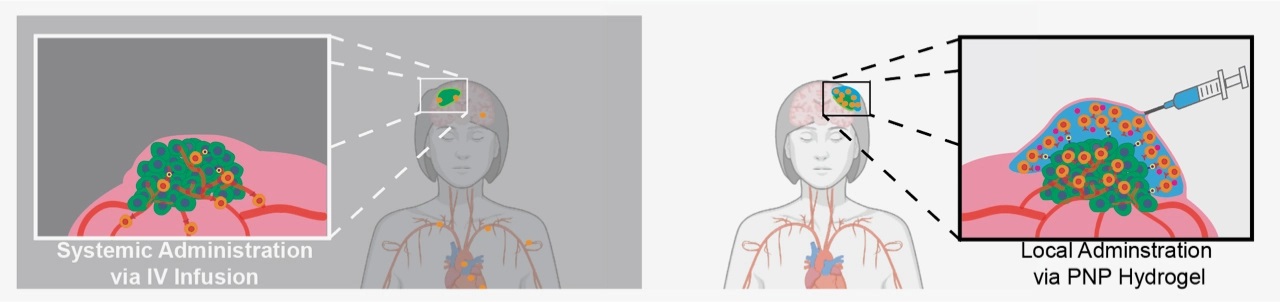
Con la administración intravenosa de las terapias CAR-T que se utiliza actualmente, la terapia circula por el torrente sanguíneo y, según los autores de este estudio, no es el enfoque ideal para tratar tumores sólidos. Este tipo de tumores suelen ser densos, se ubican en lugares muy específicos y tiene capacidad para “esconderse y defenderse” de las células inmunitarias. Todo esto hace que “las células CAR-T tengan dificultades para infiltrarse y atacar ese tumor”, apunta Abigail Grosskopf, autora principal del estudio.
La administración intravenosa de las terapias CAR-T que se utiliza actualmente no es el enfoque ideal para tratar tumores sólidos
El papel de las citoquinas y cómo aumentar su cantidad
Para activar las células CAR-T lo suficiente como para que puedan erradicar un tumor deben estar expuestas de forma prolongada a una alta concentración de las proteínas de señalización o citoquinas. Estas son las que indican a las células T reprogramadas que se repliquen rápidamente y se preparen para destruir el tumor. Sin embargo, si se administra sistémicamente a través de un goteo intravenoso, la cantidad de citoquinas requerida para lanzar un ataque efectivo sería tóxica para otras partes del cuerpo.

¿Cómo resolver este problema? Grosskopf y sus colegas crearon un gel hecho de agua, de un polímero de celulosa y de nanopartículas biodegradables. Es uno de los “grandes beneficios” de esta sustancia, “lo fáciles que son de hacer: mezclas dos cosas y los inyectas”, cuenta la investigadora. Estos componentes se unen como un “velcro molecular”. Es decir, tienen capacidad para pegarse, pero también se pueden separar. De esta forma, el gel “se puede inyectar a través de pequeñas agujas”, explica la investigadora. “Sin embargo, una vez se ha inyectado, el velcro se encuentra de nuevo y se convierte en uan estructura de gel resistente”. Es decir, una vez se ha inyectado en forma líquida a través de la aguja, los materiales forman un gel sólido.
Dentro de esta estructura, que tiene una configuración similar a la de una malla, las células inmunitarias crecen y proliferan. Pero también se van liberando de forma continua para atacar el tumor.
Dentro de esta estructura, que tiene una configuración similar a la de una malla, las células inmunitarias crecen y proliferan. Pero también se van liberando de forma continua para atacar el tumor. Las citoquinas quedan dentro de la malla, pero las conexiones de esta estructura no son tan fuertes como para que las CAR-T no las pueda romper cuando estén listas para eliminar las células cancerosas.
Administración en ratones y resultado
El equipo de investigadores puso a prueba su método en ratones con tumores sólidos. Vieron que todos los ratones a los que habían inyectado el gel junto al tumor quedaron libres de cáncer tras 12 días. Además, compararon esta forma de administrar la terapia celular con la aplicación mediante goteo intravenoso o en solución salina en vez de en gel y vieron que era menos efectivo en los tumores.
Vieron que todos los ratones a los que habían inyectado el gel junto al tumor quedaron libres de cáncer tras 12 días
También probaron a introducir en el gel solamente las CAR-T, sin citoquinas. El resultado es que los tumores desaparecieron más lentamente o no desaparecieron en absoluto en algunos ratones. En cuanto a su seguridad, el gel no provocó reacciones inflamatorias adversas en los ratones. Además, se degradó totalmente dentro del cuerpo en pocas semanas.
También probaron a inyectar el hidrogel más lejos del tumor. “Para sorpresa de todos”, los tumores desaparecieron, aunque llevó el doble de tiempo que cuando se inyectó junto al cáncer
El equipo también probó a inyectar el gel de tratamiento más lejos del tumor, en el lado opuesto al crecimiento canceroso en el cuerpo del ratón. Según destaca la Universidad de Oxford, “para sorpresa de todos”, los tumores de los animales desaparecieron, aunque llevó el doble de tiempo que cuando se inyectó junto al cáncer. “Estamos evaluando principalmente tumores en los que podemos inyectar el gel junto a ellos”, apunta Appel.
“Pero, lamentablemente todavía no podemos llegar a todos los tejidos del cuerpo. Así, esta capacidad para inyectar lejos de los tumores posiblemente abre la puerta a tratar cualquier tumor sólidos“, añade. Precisamente, los próximos experimentos preclínicos del laboratorio se centrarán en explorar la capacidad de este método para tratar tumores lejanos. “Necesitamos hacer más trabajo preclínico, pero creo que es muy prometedor”, afirma, esperanzada, Grosskopf.
Noticias complementarias
- El 12 de Octubre inicia este año el ensayo con sus células Stab, una «evolución» de las CAR-T «más efectiva»
- España participa en 24 ensayos clínicos con CAR-T, el 17% académicos
- Dr. Juan Luis Reguera: «Hay que mejorar la formación para que cualquier paciente se pueda beneficiar del tratamiento con CAR-T”
- Dra. Anna Sureda: “Los resultados que se están consiguiendo con células CAR-T modificarán la manera de utilizar los trasplantes»