..Redacción.
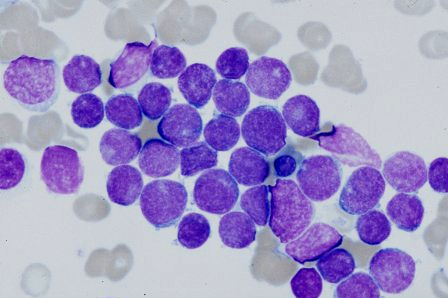
Kite, una compañía de Gilead, ha anunciado que la Comisión Europea ha aprobado su terapia de células CAR-T brexucabtagén autoleucel (Tecartus) para el tratamiento de pacientes adultos de 26 años o más con leucemia linfoblástica aguda (LLA) de precursores de células B en recaída o refractaria (r/r). La leucemia linfoblástica aguda (LLA) es un tipo agresivo de cáncer de la sangre; y la forma más común es la LLA de precursores de células B.
La leucemia linfoblástica aguda es un tipo de tumor agresivo de cáncer en la sangre
Christi Shaw, CEO de Kite, ha destacado que “esta es la cuarta indicación en Europa para la que se aprueba una terapia de Kite, lo que demuestra claramente los beneficios que ofrecen a los pacientes, especialmente para aquellos con opciones de tratamiento limitadas”. Esta aprobación está respaldada por los datos del estudio internacional de fase 1/2 ZUMA-3 en pacientes adultos con LLA en recaída o refractaria.
Esta nueva indicación refuerza el valor de la terapia celular brexucabtagén autoleucel. La terapia ya recibió aprobación europea el pasado diciembre de 2020 para pacientes adultos con linfoma de células del manto en recaída o refractario después de dos o más líneas de terapia sistémica, incluido un inhibidor de tirosina-quinasa de Bruton. Las terapias CAR-T son una realidad en España desde hace más de tres años gracias al Plan Nacional de Abordaje de Terapias Avanzadas.
Noticias complementarias
- Europa aprueba un nuevo tratamiento antirretroviral para personas con VIH multirresistente
- Cáncer de mama triple negativo metastásico: 25 líderes de opinión conciencian sobre las necesidades urgentes de las pacientes
- Curación, muerte súbita y la nueva variante aislada en Holanda, últimos focos de investigación en VIH